Бухнера — Курциуса — Шлоттербека реакция
БУХНЕРА — КУРЦИУСА — ШЛОТТЕРБЕКА РЕАКЦИЯ
получение карбонильных соед. и замещенного оксирана взаимод. альдегида или кетона с диазосоединением, напр.:
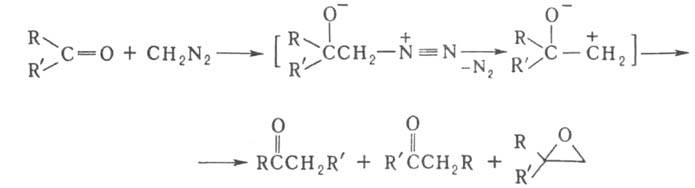
Процесс обычно осуществляют при комнатной или более низкой температуре в эфире, иногда с применением катализаторов, напр. H2O, спиртов, LiCl. В качестве диазосоединений обычно используют диазометан, диазоуксусный эфир и этиловый эфир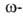 диазокротоновой кислоты. В некоторых случаях диазосоединение получают в ходе реакции из нитрозоалкилуретанов ROC(O)N(NO)(R') в присутствии основания в среде метанола.
диазокротоновой кислоты. В некоторых случаях диазосоединение получают в ходе реакции из нитрозоалкилуретанов ROC(O)N(NO)(R') в присутствии основания в среде метанола.
Направление реакции зависит от строения карбонильного соединения. Обычно образуется смесь трех продуктов. Электроноакцепторные заместители в α-положении к карбонильной группе ускоряют реакцию и повышают выход замещенного оксирана, электронодонорные — карбонильных соединений. Ациклич. кетоны реагируют медленнее альдегидов и, кроме того, приводят к большему выходу оксиранов.
В случае алициклич. кетонов основная реакция — расширение цикла, напр.:
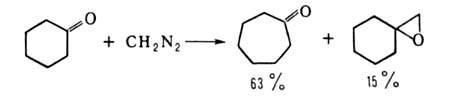
При использовании α-метил- и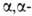 диметилциклопентанонов и циклогексанонов выход кетона достигает 96%.
диметилциклопентанонов и циклогексанонов выход кетона достигает 96%.
При использовании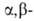 непредельных альдегидов или кетонов диазосоединение присоединяется по кратной связи с образованием замещенного 1-пиразолина:
непредельных альдегидов или кетонов диазосоединение присоединяется по кратной связи с образованием замещенного 1-пиразолина:
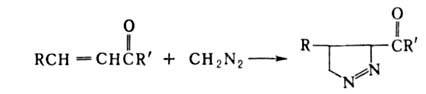
В случае 1,2-дикарбонильных соед. образуется циклич. диэфир, напр.:
Побочные процессы в реакции — полимеризация диазосоединения и его взаимод. с образующимися карбонильными соединениями.
Реакция открыта Э. Бухнером и Т. Курциусом в 1885, позднее подробно изучалась Ф. Шлоттербеком.
Лит.: Гутше К., в сб.: Органические реакции, пер. с англ., сб. 8, М., 1956, с. 469–559.
Н. Э. Нифантьев
