комплексы металлов с радикальными лигандами
КОМПЛЕКСЫ МЕТАЛЛОВ С РАДИКАЛЬНЫМИ ЛИГАНДАМИ
содержат в координац. сфере металла в качестве лигандов своб. радикалы. Наиб. изучены комплексы с пространственно-затрудненными нитроксильными, феноксильными и семихиноновыми лигандами. По типу связи металл-лиганд выделяют две основные группы. К первой относятся комплексы, в которых металл непосредственно не взаимод. с радикальным центром и связь металла с лигандом осуществляется σ- или π-связями, а также с участием неподеленных электронных пар. К этой группе относятся соед. с нитроксильными и феноксильными лигандами, содержащими функц. группы, такие как азометиновая, ксантогенатная, дипиридильная, β-дикетонатная, аллильная, порфириновая и др., напр.:
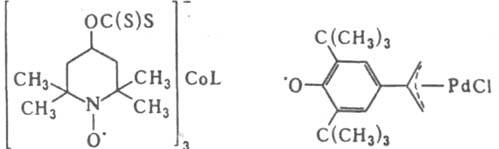
L — разл. лиганды в координац. сфере металла. Комплексы с нитроксильными лигандами получают реакциями без затрагивания своб. валентности лиганда, которые осуществляются традиционными для каждой функц. группы синтетич. методами, а с феноксильными — окислением диамагнитных комплексов металлов, содержащих лиганды с фенольными группами. Методом ЭПР в комплексах этой группы обнаружено незначит. изменение распределения спиновой плотности по сравнению со своб. лигандом. В комплексах, содержащих 2–4 радикальных лиганда, обнаружен спиновый обмен неспаренных электронов лигандов, скорость которого определяется структурой комплекса и природой металла; в комплексах, содержащих парамагнитные ионы металла, — обмен неспаренных электронов лиганда и металла. Ко второй группе относятся комплексы, в которых связь металл — лиганд осуществляется взаимод. орбитали радикального центра с вакантными орбиталями атома металла, напр. относительно неустойчивые комплексы нитроксильных радикалов с кислотами Льюиса (см. формулу I). К этой группе относятся также орто-семихиноновые системы, которые в зависимости от природы металла и его лигандного окружения могут находиться в виде ионных пар (формула II), феноксильных радикалов (III), в которых возможна миграция металлоорг. фрагмента между атомами О
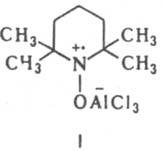
лиганда, хелатных комплексов (IV), в которых атом металла связан с атомами О лиганда тремя электронами, и комплексов со своб. валентностью на атоме металла (V):
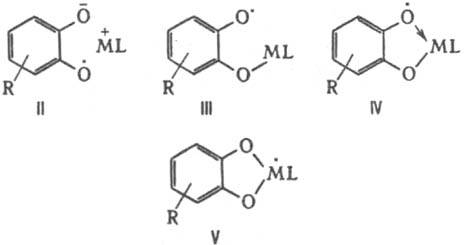
Между этими структурами возможен переход, зависящий от природы лигандного окружения металла. Полилкгандные семихиноновые комплексы могут существовать в виде монорадикалов, анион-радикалов и полирадикалов; для каждой из них возможен внутримол. обмен своб. валентности и связи ("блуждающая валентность"), напр.:
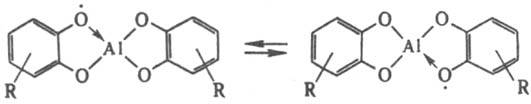
Семихиноновые комплексы получают взаимод. активных форм элементов II-IV гр. периодической системы (напр., амальгамы металлов, белый Р, желтый As) или металлоорг. соед. с орто-хинонами, а также обменными реакциями семихинолятов щел. металлов с галогенидами др. элементов.
Лит.: Абакумов Г.А., "Ж. Всес. хим. общества им. Д.И. Менделеева", 1979, т. 24, № 2, с. 156–60; Милаева Е.Р. [и др.], "Успехи химии", 1982, т. 51, в. 10, с. 1638–73; Кабачник М.И. [и др.], в сб.: Итоги науки и техники. Сер. Органическая химия, т. 5, М., 1984, с. 3–130.
А. И. Прокофьев
