кремния хлориды
КРЕМНИЯ ХЛОРИДЫ (хлорсиланы)
SiX.Cl4-n где Х-Н, Br, I, F, n=0,1,2,3, бесцв. соед. с резким запахом. Связь Si—Cl устойчива к гомолитич. разрыву и легко расщепляется ионными, особенно нуклеофильными, агентами. К. х. хорошо раств. в органических растворителях. Водой в большинстве случаев гидролизуются с образованием геля SiO2 и HCl. Реакции со спиртами, фенолами и аминами приводят к соответствующим алкокси-, арокси- и аминопро-нз водным. Тетрахлорид (тетрахлорсилан) SiCl4 — бесцветная жидкость, дымящая на воздухе; ΔH0исп 30 кДж/моль, ΔH0обр −662,2 кДж/моль; S0298 67,495 Дж/(моль∙К); уравнение температурной зависимости давления пара: lgp( мм рт. ст.)= 7,494-1524/T в интервале 298,2–340,9 К (см. также табл.).
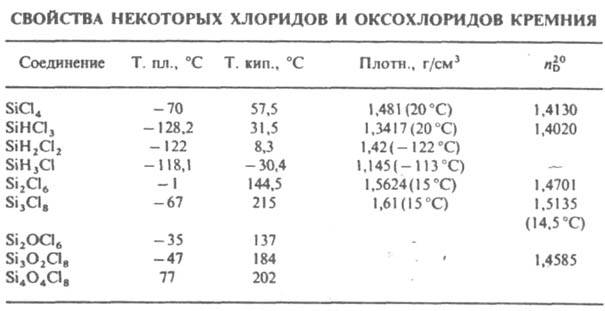
Образует аддукты с триметил-, этил-, диэтил- и триэтиламинами, анилином и его производными. В промышленности SiCl4 получают хлорированием ферросилиция при 700 °C, в лаборатории — хлорированием Si или смеси кремнезема, обугленного крахмала и угля при нагр., действием фосгена на кремнезем в присутствии сажи при 700–1000 °C. Тетрахлорид — исходное вещество в производстве эфиров ортокремниевой кислоты, аэросила, кремнийорг. мономеров в производстве термостойких пластмасс, смазочных масел, электроизоляц. материалов, при получении хим. осаждением из газовой фазы особо чистых кварцевых стекол, а также при послойном осаждении заготовок волоконных световодов. В смеси с NH3 использовался в 1-ю мировую войну как дымообразователь. Трихлорсилан (силикохлороформ) SiHCl3 — жидкость, дымящая на воздухе. Дает аддукты с триметиламином, пиридином, ТГФ. Получают взаимод. Si с HCl при 280–320 °C в псевдоожиженном слое, восстановлением SiCl4 водородом при 1000–1100 °C, как побочный продукт в производстве алкил- и арилтрихлорсиланов. Трихлорсиланисходное вещество в производстве винил-, фенил-, аллил-, гексил- и нонилтрихлорсиланов, триэтоксилана (применяемого для получения полупроводникового Si высокой чистоты), поликристаллич. Si путем восстановления водородом при 1000–1200 °C. Горюч. ПДК 1 мг/м3. Известны гомоцепные SinCl2n+2 и циклич. SinCl2n хлорполисиланы, оксохлориды Si (хлорсилоксаны) общей формулы SinOn_1Cl2n+2, имеющие линейные или разветвленные молекулы, или формулы (SinОnCl2n)x, имеющие циклич. структуру. Известны низшие газообразные К.х. SiCl, SiCl2 и SiCl3. К. х. раздражают верх, дыхат. пути и слизистые оболочки в результате выделения HCl; вещества, содержащие группы SiH, с воздухом образуют взрывоопасные смеси.
Лит.: Лапидус И.И., Нисельсон Л. А., Тетрахлорсилан и Трихлорсилан, М., 1970; Хананашвили Л.М., Андрианов К.А., Технология элементоорганических мономеров и полимеров, 2 изд., М., 1983.
В. Н. Емельянов
