тетрахлорэтилен
ТЕТРАХЛОРЭТИЛЕН (перхлорэтилен) CCl2 = CCl2
мол. м. 165,83; бесцветная жидкость с резким запахом; т. пл. −22,4 °C, т. кип. 121 °C; 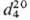 1,625;
1,625; 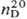 1,5044; tкрит 340 °C, pкрит 4,49 МПа, dкрит 0,573 г/см3; η (мПа∙с) жидкости 1,41 ( −20 °C), 0,88 (20 °C), 0,44 (100 °C), η (мкПа∙с) пара 8,55 (20 °C), 11,20 (100 °C); γ (мН/м) 31,7 (20 °C), 22,6 (100 °C); давление пара (кПа) 0,13 ( −20,1 °C), 0,66 (0 °C), 1,86 (20 °C), 12,42 (60 °C), 53,32 (100 °C); С0р кДж/(кг∙К) жидкости 0,753 (_40 °C), 0,858 (20 °C), 0,962 (100 °C), пара 0,573 (0 °C), 0,620 (100 °C), 0,665 (300 °C);
1,5044; tкрит 340 °C, pкрит 4,49 МПа, dкрит 0,573 г/см3; η (мПа∙с) жидкости 1,41 ( −20 °C), 0,88 (20 °C), 0,44 (100 °C), η (мкПа∙с) пара 8,55 (20 °C), 11,20 (100 °C); γ (мН/м) 31,7 (20 °C), 22,6 (100 °C); давление пара (кПа) 0,13 ( −20,1 °C), 0,66 (0 °C), 1,86 (20 °C), 12,42 (60 °C), 53,32 (100 °C); С0р кДж/(кг∙К) жидкости 0,753 (_40 °C), 0,858 (20 °C), 0,962 (100 °C), пара 0,573 (0 °C), 0,620 (100 °C), 0,665 (300 °C); 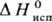 241,8 кДж/кг,
241,8 кДж/кг, 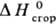 −679,9 кДж/моль,
−679,9 кДж/моль, 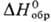 −15,06 кДж/моль; теплопроводность [Вт/(м∙К)] жидкости 0,1213 ( −20 °C), 0,1109 (20 °C), 0,0910 (100° С), пара 0,00875 (121 °C); ε 2,2 (20 °C). Хорошо раств. в органических растворителях. Растворимость в воде 0,04% по массе (25 °C), воды в Т. 0,008%. Образует азеотропную смесь с водой (т. кип. 87,7 °C, 15,8% воды).
−15,06 кДж/моль; теплопроводность [Вт/(м∙К)] жидкости 0,1213 ( −20 °C), 0,1109 (20 °C), 0,0910 (100° С), пара 0,00875 (121 °C); ε 2,2 (20 °C). Хорошо раств. в органических растворителях. Растворимость в воде 0,04% по массе (25 °C), воды в Т. 0,008%. Образует азеотропную смесь с водой (т. кип. 87,7 °C, 15,8% воды).
При взаимодействии Т. с хлором в жидкой фазе в присутствии 0,1% РеCl3 при 50–80 °C образуется гексахлорэтан, при взаимодействии с Cl2 и HF в присутствии SbCl5-хладон 113. Гидролиз Т. (особенно в присутствии H2SO4) приводит к трихлоруксусной кислоте, гидрирование (кат.—Ni, Pd, Pt) — к тетрахлорэтану, окисление O2 воздуха — к трихлорацетилхлориду и фосгену. Для стабилизации используют N-метилпиррол, N-метил-морфолин и др.
Получают Т. (совместно с CCl4): исчерпывающим хлорированием индивидуальных углеводородов C1-C3 или их смесей либо соответствующих хлоруглеводородов в паровой фазе при 600 °C; хлорированием смеси производных пропана, пропилена и хлоруглеводородов C3 в кипящем слое песка при 520–540 °C; окислит. хлорированием углеводородов C2 — C3, их хлорпроизводных или их смесей (кат. — CuCl2 + KCl на корунде, силикагеле или др. носителе) при 350–400 °C.
Применяют Т. для хим. чистки одежды, обезжиривания металлов, в качестве растворителя в текстильной промышленности, для производства хладона 113.
Т. негорюч, не самовоспламеняется, невзрывоопасен. При длит. контакте оказывает токсич. действие на центр. нервную систему и печень; ПДК 10 мг/м3.
Мировое производство 700 тыс. т/год (1990).
Лит. см. при ст. тетрахлорэтаны.
Ю. А. Трегер
Значения в других словарях
- тетрахлорэтилен — орф. тетрахлорэтилен, -а Орфографический словарь Лопатина
- ТЕТРАХЛОРЭТИЛЕН — ТЕТРАХЛОРЭТИЛЕН (перхлорэтилен) — Cl2C=CCl2, бесцветная жидкость, tкип 121 °С. Растворитель и экстрагирующий агент, напр., для каучуков, пластмасс, жиров. Используется при химической чистке одежды. Большой энциклопедический словарь
