тиопираны
ТИОПИРАНЫ
мол. м. 98,10. Различают α-Т. (2H-Т.; формула I) и γ-T. (4H-Т.; II). Незамещенные и монозамещенные Т. неустойчивы на воздухе, темнеют и расплываются; ди- и полизамещенные-устойчивые вещества.
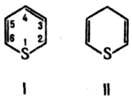
Незамещенные Т. — светло-желтые жидкости: для α-Т. т. кип. 32–34 °C/12 мм рт. ст., 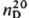 _ 1,5198; для γ-T. т. кип. 30 °C/12 мм рт. ст.,
_ 1,5198; для γ-T. т. кип. 30 °C/12 мм рт. ст., 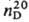 1,5623. Замещенные Т. — гл. обр. бесцветные кристаллы; для 2,3,4-три- фенил-6-трет-бутил-α-T. т. пл. 127–128 °C, для 2,4,6-трифенил-γ-Т. 104–106 °C. Т. раств. в этаноле, диэтиловом эфире, ацетоне, не раств. в воде.
1,5623. Замещенные Т. — гл. обр. бесцветные кристаллы; для 2,3,4-три- фенил-6-трет-бутил-α-T. т. пл. 127–128 °C, для 2,4,6-трифенил-γ-Т. 104–106 °C. Т. раств. в этаноле, диэтиловом эфире, ацетоне, не раств. в воде.
В ИК спектре характеристич. частоты поглощения для α-Т. 1535, 1565 (vC=C) см−1, для γ-T. 1600, 1620–1640 (vC=C) см−1.
С трифенилперхлоратом в присутствии галогенов Т. образуют тиопирилия соли, под действием протонных и апротонных кислот диспропорционируют с образованием солей тиопирилия, дигидротиопирана и тетрагидротиопирана (тиациклогекса-на), напр.:
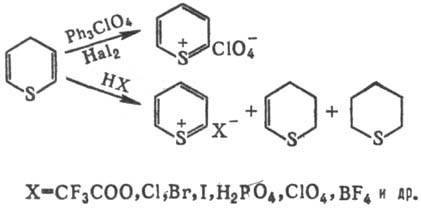
Т. присоединяют по двойным связям Br2, дихлоркарбен, водород (при каталитич. гидрировании или восстановлении по Клеменсену). Полизамещенные и конденсированные Т. с H2O2 и др. окислителями образуют сульфоны или сульф-оксиды; незамещенные в положении 4 γ-T. под действием MnO2 окисляются до тиопиронов.
Под действием NaNH2 в жидком NH3 и бутиллития в ТГФ Т. образуют соли тиопиранида, напр.:

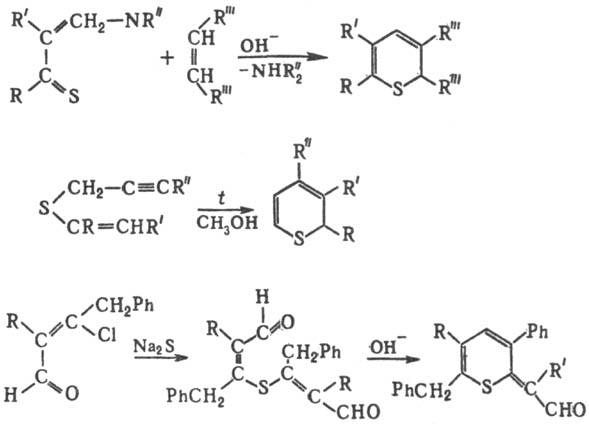
α-Т. и его производные получают по реакциям:
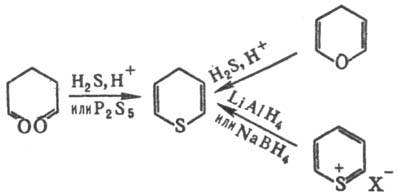
γ-T. и его производные синтезируют из 1,5-дикарбонильных соед., пиранов, солей тиопирилия по реакциям, напр.:
Лит.: Харченко В. Г., Чалая С. Н., Коновалова Т. М., "Химия гетероцикл. соединений", 1974, №9, с. 1155–70; Харченко В. Г., Чалая С. Н., Тиопираны, соли тиопирилия и родственные соединения, Саратов, 1987.
В. Г. Харченко, С. Н. Чалая
