ацетиленовые комплексы переходных металлов
АЦЕТИЛЕНОВЫЕ КОМПЛЕКСЫ ПЕРЕХОДНЫХ МЕТАЛЛОВ
π-комплексы, содержащие в качестве лиганда ацетилен или его производные. Связь между атомом металла и лигандом осуществляется перекрыванием вакантной орбитали металла со связывающей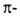 орбиталью ацетилена (связь донорно-акцепторного типа) и заполненной d-орбитали металла с разрыхляющей
орбиталью ацетилена (связь донорно-акцепторного типа) и заполненной d-орбитали металла с разрыхляющей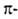 орбиталью ацетилена (дативная связь).
орбиталью ацетилена (дативная связь).
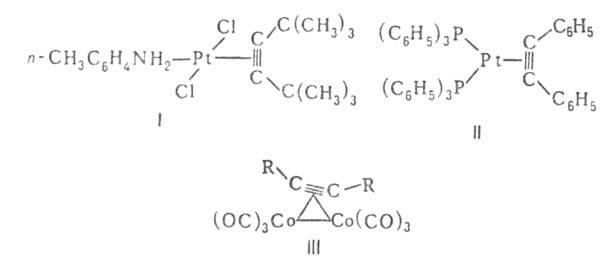
Координиров. ацетилен имеет искаженную цис-конфигурацию (заместители повернуты в сторону от атома металла). Связь C—C в комплексе длиннее, чем в своб. ацетилене; частота валентных колебаний координированной тройной связи понижена. Степень искажения молекулы ацетилена при координации с металлом тем больше, чем значительнее вклад дативной компоненты в связь металл--ацетилен. В комплексах Pt(II), Pd(II), Cu(I), Ag(I) и Au(I) тройная связь искажена слабо (комплексы 1-го типа; напр., формула I), в комплексах металлов V-VIII групп, находящихся в низших степенях окисления (0, +1), — существенно (комплексы 2-го типа; типичный представитель — соед. формулы II). Величина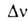 , т. е. разность частот валентных колебаний тройной связи C≡C в своб. ацетилене и в комплексах, составляет в первом случае ок. 200см−1, во втором — ок. 450см−1. Молекула ацетилена может координироваться одновременно с двумя атомами металла, образуя мост между ними (напр., формула III). Ацетиленовый лиганд м. б. связан с металлич. кластером.
, т. е. разность частот валентных колебаний тройной связи C≡C в своб. ацетилене и в комплексах, составляет в первом случае ок. 200см−1, во втором — ок. 450см−1. Молекула ацетилена может координироваться одновременно с двумя атомами металла, образуя мост между ними (напр., формула III). Ацетиленовый лиганд м. б. связан с металлич. кластером.
В би- и полиядерных комплексах искажение координированного ацетилена выражено сильнее, чем в моноядерных; Av составляет ~ 600 см−1. Известны комплексы, содержащие два или более независимо координированных ацетиленовых лиганда; примерами могут служить соед. Mo и W общей формулы [ML(RC≡CR)3], где L = CO или CH,CN, соед. Ni и Pd-[M4(CO)4(CF3C≡CCF3)3].
Координация с металлом стабилизирует ацетиленовые соед., не способные существовать в своб. состоянии, напр. циклические с малым размером цикла и дегидробензол. Получены комплексы Pt и Pd состава [M(PPh3)2(ac)], где ас-циклогексин или циклогептин, а также комплексы Nb и Та с дегидробензолом и др.
Комплексы Cu(I), Ag(I) и Au(I) легко диссоциируют на исходные компоненты, комплексы Pt(II) разлагаются лишь при высокой температуре. Из А. к. п. м. второго типа наиб. прочны [Pt(R3'E)2(RC≡CR)1 где Е=Р, As, а также [Co2(CO)6(RC≡CR)] и [(C5H5Ni)2(RC≡CR)]; устойчивость их повышается с возрастанием электроноакцепторно-го характера заместителей в ацетиленовом лиганде.
Ацетиленовые комплексы способны к разл. превращениям. Например, комплексы Cu(I) с ацетиленом и его моноза-мещенными под действием водного раствора NH3 или воды превращ. в ацетилениды RC≡CCu; комплексы Pt(0) с некоторыми дизамещенными ацетиленами в результате окислит. присоединения образуют ацетилениды:
 , где X = Y = CN или Х = С1 и Y = Ph.
, где X = Y = CN или Х = С1 и Y = Ph.
Ацетиленовые комплексы Pt(0) и ряда др. металлов присоединяют в мягких условиях молекулу кислоты, в частности HCl; при этом образуются винильные производные, напр. [Pt(PPh3),(Cl)(RC=CHR)].
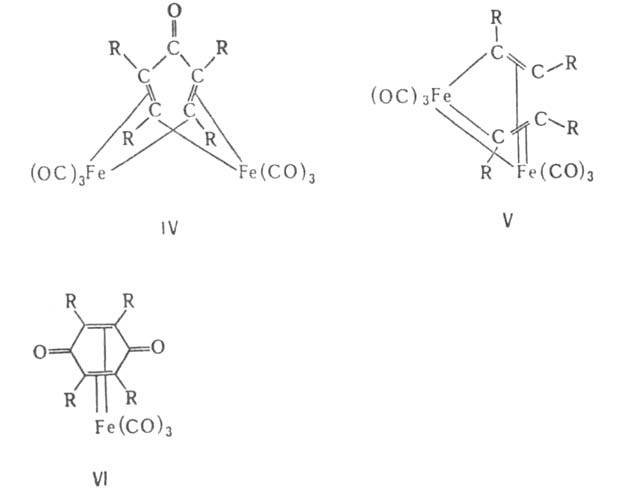
Наиб. характерна для координиров. ацетиленов циклоолигомеризация, приводящая к возникновению новых связей C—C. Участие атома металла и координированных с металлом лигандов (в т. ч. карбонильных) приводит к образованию циклов с σ-связями М—С, соединений ряда циклопентадиенона, хинона и др. Образующиеся продукты выделяются в своб. состоянии либо сохраняют связь с металлом. Так, при действии ацетиленов, а также при нагр. из комплексов [Fe2(CO)6(RC ≡ CR)] получены железоорг. соединения формул IV-VI и своб. хиноны. Общий метод синтеза А. к. п. м. основан на замещении ацетиленом разл. лигандов, напр.:
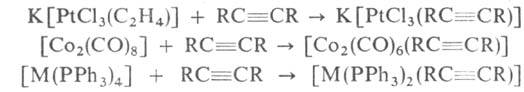 ,
,
где М = Pt, Pd. Комплексы Cu(I), Ag(I) и Au(I) получают взаимод. ацетиленов с солями металлов, напр.: CuCl + C2H2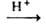 C2H2(CuCl)n Др. методы синтеза — присоединение ацетиленов к координационно-ненасыщенным соед., напр. [Pt(PPh3)2l [(C5H5)2V], с образованием соотв. [Pt(PPh3)2(RC ≡ CR)], [(C5H5)2V(RC ≡ CR)]; восстановление соед. металлов в высшей степени окисления в присутствии ацетиленов: [цис-PtCl2(PPh3)2] + N2H4 + RC ≡ CR → [Pt(PPh3)2(RG ≡ CR)]; взаимод. ацетиленов с атомами металлов. Так, при реакции CF3C ≡ CCF3 с атомами Pd и Ni при −196 °C с послед, обработкой CO образуются комплексы [M4(CO)4(CF3C ≡ CCF3)3].
C2H2(CuCl)n Др. методы синтеза — присоединение ацетиленов к координационно-ненасыщенным соед., напр. [Pt(PPh3)2l [(C5H5)2V], с образованием соотв. [Pt(PPh3)2(RC ≡ CR)], [(C5H5)2V(RC ≡ CR)]; восстановление соед. металлов в высшей степени окисления в присутствии ацетиленов: [цис-PtCl2(PPh3)2] + N2H4 + RC ≡ CR → [Pt(PPh3)2(RG ≡ CR)]; взаимод. ацетиленов с атомами металлов. Так, при реакции CF3C ≡ CCF3 с атомами Pd и Ni при −196 °C с послед, обработкой CO образуются комплексы [M4(CO)4(CF3C ≡ CCF3)3].
Ацетиленовые комплексы — промежут. продукты при превращ. ацетиленов с участием соед. переходных металлов. О σ-комплексах переходных металлов с ацетиленами (ацетиленидах) см. комплексы переходных металлов с σ-связью металл-углерод.
Лит.: Юрьева Л.П., в кн.: Методы элементоорганической химии. Типы металлоорганических соединений переходных металлов, под ред. А. Н. Несмеянова и К. А. Кочешкова, кн. 1. М., 1975, с. 384–514.
Л. Л. Юрьева
