ацетонциангидрин
АЦЕТОНЦИАНГИДРИН (α-гидроксиизобутиронитрил, нитрил α-гидроксиизомасляной кислоты) (CH3)2C(OH)CN
мол. м. 85,11; бесцветная жидкость; т. затв. −19 °C, т. кип. 81 °C/15 мм рт. ст., т. разл. 120 °C; d420 0,930, nD20 1,3992; уравнение температурной зависимости давления пара в интервале 50–110 °C: Ig p (мм рт. ст.) = 9,8457 — 3054,3/Т(К); μ 10,575∙10−30 Кл∙м (бензол); Cр (жидкость) 145,3 Дж/(моль∙К); ΔHисп 47,5 кДж/моль. Легко раств. в воде, спирте, эфире и др. органических растворителях, плохо — в петролейном эфире и CS2.
А. обладает хим. свойствами, характерными для гидроксинитрилов, напр. гидролизуется водными растворами HCl или H2SO4 до α-гидроксиизомасляной кислоты (CH3)2С(OH)COOH или ее амида; при действии галогенидов Р образует галогензамещенные изобутиронитрилы, при действии NH3- α-аминоизобутиронитрил (CH3)2C(NH2)CN; в присутствии кислотных катализаторов ацетилируется уксусным ангидридом. Под действием конц. H2SO4 от А. отщепляется вода и образуется метакриловая кислота CH2=C(CH3)COOH, при обработке P2O5 или SOCl2 — метакрилонитрил CH2=C(CH3)CN.
В промышленности А. получают взаимод. ацетона, который берут в избытке, с HCN в присутствии водных растворов NaOH, KOH или Na2CO3 при температуре не выше 30 °C, обычно по непрерывной схеме. Реакция экзотермична (35,2 кДж/моль). Поскольку А. в щелочной среде легко отщепляет HCN, продукт-сырец подкисляют H2SO4 до pH 1–2, отделяют от солей и подвергают ректификации. А. стабилизируют небольшим количеством H2SO4; выход 90–95%. В лаборатории А. получают добавлением 35–40%-ной H2SO4 к водному раствору ацетона и NaCN при 10–20 °C или по реакции:
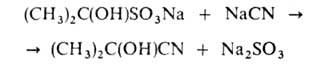
А. — сырье в производстве метакриламида, метакриловои кислоты, метилметакрилата, метакрилонитрила, азо-бис-изобутиронитрила. В лаб. орг. синтезе — источник HCN для получения циангидринов и для гидроцианирования.
А. — ферментный яд, поражающий дыхат. центры (по действию сходен с цианидами), легко всасывается через неповрежденную кожу; ПДК 0,9 мг/м3, в воде — 0,001 мг/л; ЛД50 30 мг/кг (мыши, перорально). Т. всп. 76 °C, т. воспл. 78 °C, т. самовоспл. 544 °C; КПВ 2,2–12%; температурные пределы воспламенения 38–84 °C.
Мировое производство А. превышает 500 тыс. т/год (1982).
Лит.: Бобков С.С, С.ми рнов С. К., Синильная кислота, М, 1970; Зильберман Е.Н., Реакции нитрилов, М.. 1972; Migrdichian V., The chemistry of organic cyanogen compounds, N. Y., 1947; Kirk-Qthmer encyclopedia. 3 ed., v. 15, N.Y., 1981. '
С. К. Смирнов
