адамантан
АДАМАНТАН (трицикло[3,3,1,13,7]декан) (от греч. adamas, род. падеж adamantos — твердый металл; алмаз)
мол. м. 136,23; бесцветные кристаллы с запахом камфоры; т. пл. 269 °C; легко возгоняется; d204 1,07; 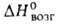 58,6 кДж/моль,
58,6 кДж/моль, 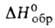 −197,2 кДж/моль; раств. в органических растворителях, не раств. в 50%-ном спиоте и воде. Углеводный скелет А. подобен структурной единице алмаза. Жесткая, но не напряженная молекула, включающая три конденсированных циклогексановых кольца в конформации кресла, обладает высокой симметрией (группа Td). При 20 °C А. имеет беспорядочную гранецентриров. кубич. структуру, переходящую при −65 °C в тетрагональную. Все длины связей С-С равны 0,154 нм, валентные углы 109,5°.
−197,2 кДж/моль; раств. в органических растворителях, не раств. в 50%-ном спиоте и воде. Углеводный скелет А. подобен структурной единице алмаза. Жесткая, но не напряженная молекула, включающая три конденсированных циклогексановых кольца в конформации кресла, обладает высокой симметрией (группа Td). При 20 °C А. имеет беспорядочную гранецентриров. кубич. структуру, переходящую при −65 °C в тетрагональную. Все длины связей С-С равны 0,154 нм, валентные углы 109,5°.
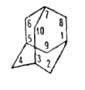
Уникальное, максимально приближенное к сферическому строение А. обусловливает особенности его свойств. Подобно алмазу, А. исключительно термостабилен (до 660 °C). Узловые атомы С (положения 1, 3, 5, 7) в А. и его производных более реакционноспособны, чем в др. мостиковых углеводородах. А. легко бромируется жидким Br2 до 1-бромадамантана. Дальнейшее бромирование, а также хлорирование действием, напр. SOCl2, CH3COCl, до 1-хлорадамантана происходит только в присутствии кислот Льюиса. Действием 95%-ной или 100%-ной HNO3 А. превращается соотв. в 1-адамантаннитрат или 1,3-адамантандинитрат, которые легко гидролизуются в 1-гидрокси- или 1,3-дигидроксиадамантан. К смеси последних приводит также окисление А. действием CrO3. Нитрование смесью HNO3-SbF5 дает 1-нитроадамантан. Алкилирование или арилирование (кат. — А1Hal3) и карбоксилирование (кат. — 8O3) приводят соотв. к 1-алкил- или 1-ариладамантану и 1-карбоксиадаман-тану, аминирование А. с помощью NC13 (кат. — кислоты Льюиса) — к 1-аминоадамантану (выход 95%). Реакц. способность А. в этих процессах определяется необычной стабильностью адамантилий-катиона, который легко образуется под действием кислот Льюиса или сильных окислителей. 1-Брома-дамантан легко гидролизуется в водно-спиртовой среде до 1-гидроксиадамантана, обменивает бром при нагревании с галогеноводородными кислотами на др. галоген. 1-Бром- и 1-гидроксизамещенные А. — исходные соед. для синтеза 1-амино-, 1-арил- и 1-карбоксиадамантанов; 2-адамантанон, образующийся при нагревании А. с конц. H2SO4, применяют для синтеза 2-гидрокси-, 2-галоген-, 2-амино- и 2-карбо-ксиадамантанов.
А. найден в нефтях некоторых месторождений в концентрации 0,0004-0,0013% по массе.
Получают А. гидрированием дициклопентадиена до эндотриметиленнорборнана (трицикло[5,2,1,02,6]декана) с послед. его изомеризацией (кат. — А1Br3, AlCl3):
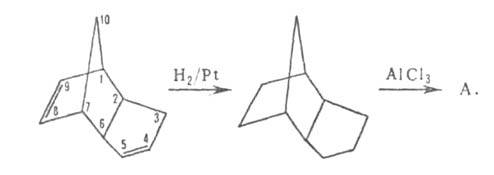
Выход 50%. Изомеризация др. полициклич. пергидроароматич. углеводородов (напр., пергидроаценафтена, пергидроантрацена, пергидрофенантрена) приводит к алкилпроизводным А.; выход до 90%.
Содержащие А. полимеры обладают высокими температурами стеклования и размягчения, низкой усадкой, прозрачностью и применяются в производстве оптич. стекол. Высоковязкие растворы полиадамантилакрилатов — загустители смазочных масел. Производные А. — лек. вещества (амантадин, ремантадин, троматадин).
А. впервые синтезирован В. Прелогом в 1941.
Лит.: Севостьянова В. В., Краюшкин М. М., Юрченко А. Г., "Успехи химии", 1970, т. 39, в. 10, а 1721–53; Хардин А. П.. Радченко С. С, там же. 1982, т. 51, в. 3, с. 480–506; Багрий Е.Н., Сагинаев А.Т., там же, 1983, г. 52, в. 9, с. 1538–67; Fort R. С, Adamantane. The chemistry of diamond molecules, N.Y., 1976.
Д. В. Иоффе, Р. Я. Попова
Значения в других словарях
- АДАМАНТАН — АДАМАНТАН (от греч. adamas, род. п. adamantos — алмаз) — бесцветные кристаллы с камфорным запахом. Структура молекулы подобна структуре алмаза. Адамантан обладает аномально высокой (для углеводородов) температурой плавления (269 °С). Большой энциклопедический словарь
