алюминия оксид
АЛЮМИНИЯ ОКСИД (глинозем) Al2O3
бесцветные кристаллы; т. пл. 2044 °C; т. кип. 3530 °C. Единственная стабильная до 2044 °C кристаллич. модификация А. о.- α-Al2O3 (корунд): решетка ромбоэдрич., а = 0,512 нм, α= 55,25° (для гексагон. установки а = 0,475 нм, с = 1,299 нм, пространственная группа D63d, z = 2); плотн. 3,99 г/см3; ΔH0пл 111,4 кДж/моль; уравнения температурной зависимости: теплоемкости C0p = = 114,4 + 12,9∙10−3Т — 34,3∙105Т2 Дж/(моль∙К) (298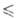 Т
Т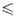 1800 К), давления пара Igp (Па) = -54800/7+1,68 (до ~ 3500 К); температурный коэф. линейного расширения (7,2–8,6)∙10−6К−1 (300
1800 К), давления пара Igp (Па) = -54800/7+1,68 (до ~ 3500 К); температурный коэф. линейного расширения (7,2–8,6)∙10−6К−1 (300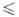 Т
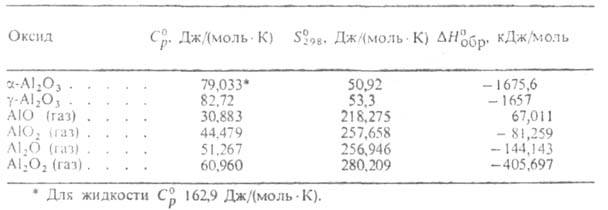
Т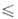 1200 К); теплопроводность спеченного при 730 °C образца 0,35 Вт/(моль∙К); твердость по Моосу 9; показатель преломления для обыкновенного луча n0 1,765, для необыкновенного пе 1,759. См. табл.
1200 К); теплопроводность спеченного при 730 °C образца 0,35 Вт/(моль∙К); твердость по Моосу 9; показатель преломления для обыкновенного луча n0 1,765, для необыкновенного пе 1,759. См. табл.
ТЕРМОДИНАМИЧЕСКИЕ СВОЙСТВА ОКСИДОВ АЛЮМИНИЯ
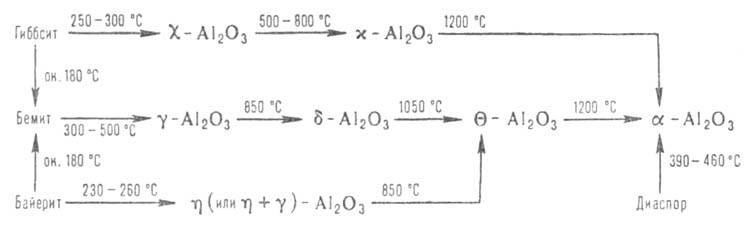
Модификация α-Al2O3 встречается в природе в виде минерала корунда, который часто содержит в растворенном виде оксиды др. металлов, придающих ему разл. окраску. Прозрачные окрашенные кристаллы-драгоценные камни (сапфиры, рубины и др.). Корунд м. б. получен искусственно в результате термич. разложения ромбич. модификации А1ООН-диаспора или полиморфных переходов метастабильных форм Al2O3 (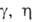 и т. д.), которые образуются при разложении кристаллич. модификаций А1(OH)3-гиббсита и байерита и AlOOH-бемита (см. алюминия гидроксид). Эти процессы м. б. представлены след. схемой:
и т. д.), которые образуются при разложении кристаллич. модификаций А1(OH)3-гиббсита и байерита и AlOOH-бемита (см. алюминия гидроксид). Эти процессы м. б. представлены след. схемой:
Модификация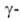 Al2O3 имеет тетрагон, кристаллич. решетку типа шпинели (а = 0,562 нм, с = 0,780нм); плотн. 3,3–3,4 г/см3; содержит структурно связанную воду в количестве 1–2%. Существует также аморфный А.о. — алюмогель, образующийся при обезвоживании гелеобразного А1(OH)3 и представляющий собой пористое, иногда прозрачное вещество.
Al2O3 имеет тетрагон, кристаллич. решетку типа шпинели (а = 0,562 нм, с = 0,780нм); плотн. 3,3–3,4 г/см3; содержит структурно связанную воду в количестве 1–2%. Существует также аморфный А.о. — алюмогель, образующийся при обезвоживании гелеобразного А1(OH)3 и представляющий собой пористое, иногда прозрачное вещество.
А. о. не раств. в воде, хорошо раств. в расплавленном криолите. Амфотерен. С NH3-H2O не реагирует. Хим. активность синтетич. А. о. сильно уменьшается с повышением температуры его получения. Прир. и искусственный (образовавшийся выше 1200 °C) корунд на воздухе при обычных условиях химически инертны и негигроскопичны. Ок. 1000 °C интенсивно взаимод. со щелочами и карбонатами щелочных металлов, давая алюминаты. Медленно реагирует с SiO2 и кислыми шлаками с образованием алюмосиликатов. При сплавлении взаимод. с KHSO4. Корунд, образовавшийся из диаспора при 500–600 °C, взаимод. также с растворами кислот и щелочей. Алюмогель и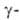 Al2O3, полученный при обжиге гидроксидов А1 при ~550 °C, весьма гигроскопичны и химически активны, реагируют с растворами кислот и щелочей.
Al2O3, полученный при обжиге гидроксидов А1 при ~550 °C, весьма гигроскопичны и химически активны, реагируют с растворами кислот и щелочей.
Сырье для получения А.о. — бокситы, нефелины, алуниты и др. (см. алюминий При соотношении в рудах Al2O3 :SiO2 > 6–7 их перерабатывают по способу Байера (осн. метод), при Al2O3 → SiO2 < 6 (высококремнистое сырье) — спеканием с известью и содой.
По способу Байера измельченный в шаровых мельницах боксит выщелачивают в автоклавах оборотным щелочным раствором алюмината Na (после выделения из него части Al2O3) при 225–250 °C. При этом алюминий переходит в раствор в виде алюмината Na. В случае бокситов, содержащих гиббсит, выщелачивание можно производить при 105 °C и обычном давлении в аппаратах с мешалкой. Алюминатные растворы разбавляют водой, отделяют шлам и подвергают разложению в аппаратах с мешалкой или эрлифтом 30–70 ч, причем выделяется ок. 1/2 образовавшегося при этом А1(OH)3. Его отфильтровывают и прокаливают во вращающихся печах или в кипящем слое при ~ 1200 °C. В результате получается глинозем, содержащий 15–60% α- Al2O3. Маточный раствор упаривается и поступает на выщелачивание новой партии боксита.
По второму способу высококремнистую измельченную руду (нефелин и др.) смешивают с содой и известняком и спекают во вращающихся печах при 1250–1300 :С. Полученную массу выщелачивают водным щелочным раствором, раствор алюмината Na отделяют от шлама, затем освобождают от SiO2, осаждая его в автоклаве при давлении ок. 0,6 МПа, а затем известью при атмосферном давлении, и разлагают алюминат газообразным CO2. Полученный А1(OH)3 отделяют от раствора и прокаливают при температуре ок. 1200 °C. При переработке нефелина, помимо глинозема, получают Na2CO3, K2CO3 и цемент. При производстве глинозема из алунитов одновременно получают H2SO4 и K2SO4. Алунитовую руду обжигают при 500–580 °C в восстановит. атмосфере и обрабатывают раствором NaOH по способу Байера. Монокристаллы выращивают зонной плавкой, по методу Вернейля или Чохральского.
Синтетич. α-Al2O3-промежут. продукт в производстве А1 (осн. область использования), огнеупорный и абразивный материал. Его применяют также при получении керамич. резцов, электротехн. керамики. Монокристаллы-лазерный материал, опорные камни часовых механизмов, ювелирные камни. Прир. корунд-абразивный (корундовые круги, наждак) и огнеупорный материал. Алюмогель, 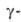 Al2O3 и его смесь с
Al2O3 и его смесь с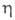 -Al2O3 — адсорбенты для осушки газов (напр., H2, Ar, C2H2) и жидкостей (ароматич. углеводородов, керосина и др.), в хроматографии; катализаторы (например, дегидратации спиртов, изомеризации олефинов, разложения H2S); носители для катализаторов (напр., Со-MoO3, Pd, Pt).
-Al2O3 — адсорбенты для осушки газов (напр., H2, Ar, C2H2) и жидкостей (ароматич. углеводородов, керосина и др.), в хроматографии; катализаторы (например, дегидратации спиртов, изомеризации олефинов, разложения H2S); носители для катализаторов (напр., Со-MoO3, Pd, Pt).
Мировое производство А. о. ок. 30 млн. т/год (1980). Известны также и другие А. о. (см. табл.), существующие в газовой фазе.
Лит.: Чалый В. П., Гидроокиси металлов. К.. 1972; Строение и свойства адсорбентов и катализаторов, пер. с англ., М., 1973: Производство глинозема. 2 изд., М., 1978; Запол ьский А.К., Сернокислотная переработка высококремнистого алюминиевого сырья. К, 1981.
Н. А. Калужский, Ю. А. Волохов
Значения в других словарях
- АЛЮМИНИЯ ОКСИД — АЛЮМИНИЯ ОКСИД (глинозем) — Al2O3, бесцветные нерастворимые в воде кристаллы, tпл 2044 °С. Получают из бокситов, нефелинов, каолина, алунитов. Сырье в производстве алюминия, катализатор, адсорбент, огнеупорный и абразивный материал. См. также Корунд, Рубин, Сапфир. Большой энциклопедический словарь
