аминодифениламины
АМИНОДИФЕНИЛАМИНЫ
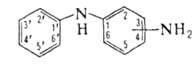
мол. м. 184,24; бесцветные кристаллы. Для 2-А. (N-фенил-1,2-диаминобензол, N-фенил-о-фенилендиамин, о-семидин) т. пл. 79–80 °C; хорошо раств. в воде, бензоле, ацетоне, хлороформе, трудно — в лигроине. Для 3-А. (N-фенил-1,3-диаминобензол, N-фенил-м-фенилендиамин) т. пл. 76–77 °C, т. кип. 190 °C/2 мм рт. ст.; хорошо раств. в воде, очень хорошо — в большинстве орг. растворителей. 4-А. (N-фенил-1,4-диаминобензол, N-фенил-n-фенилендиамин, м-семидин) полиморфен; т. пл. 66–67 и 74–75 °C, т. кип. 354 °C (в токе H2), 170 °C/1 мм рт. ст.; плохо раств. в воде, хорошо — в спирте, эфире, раств. в лигроине; ПДК 2 мг/м3.
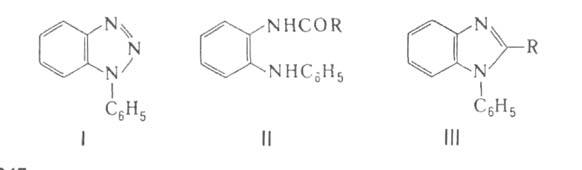
А. обладают всеми свойствами ароматич. аминов. Для них характерен также ряд специфич. свойств. 2-А. при нагр. с NaNO2 в разб. HCl превращается в 1-фенилбензотриазол (формула I); легко ацилируется, напр. под действием (CH3СО)2O-до N-ацетил-2-А. (II; R= CH3), который при нагр. с HCl или NaOH циклизуется в 1-фенил-2-метилбензимидазол (III; R = CH3), а с HCOOH — в 1-фенилбензимидазол (III; R = Н). При перегонке с PbO 2-А. превращ. в феназин.
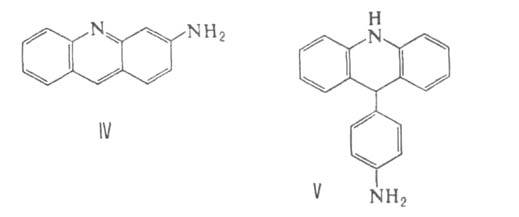
Реакция 3-А. с муравьиной кислотой при 100 °C приводит к N-формил-3-А., который при 175 °C в глицерине под действием соляной кислоты циклизуется в 3-аминоакридин (IV), а при взаимодействии с 4-аминобензальдегидом — в хризанилин (V), являющийся желто-коричневым красителем для кож.
При действии на 1 моль 4-А. 1 моля NaNO2 диазоти-руется группа NH2, при действии 2 молей — нитрозируется группа NH; нитрозированное диазосоединение устойчиво, легко вступает в азосочетание. При взаимодействии 4-А. с глицерином и конц. H2SO4 в нитробензоле (реакция Скраупа) образуется 6-анилинохинолин, при восстановит, алкилировании кетонами под давлением H2 (кат. — Ni)-N-алкил-4-А. (напр., с ацетоном-N-изопропил-4-А.).
В промышленности получают только 4-А. — восстановлением 4-нитрозодифениламина H2 (кат. — Ni) в водно-спиртовой среде в присутствии NaOH при 70–80 °C; выход 90–95%. 2-А. и 3-А. синтезируют восстановлением соответствующих ни-тродифениламинов Fe в кислой среде (напр., в CH3COOH) или H2 (кат. — Ni, Pt).
Цветная реакция на 4-А.: при смешении раствора соли 4-А. с РеCl3 образуется красная окраска, переходящая в зеленую; при больших концентрациях соли 4-А. выпадает зеленый осадок, растворяющийся в конц. H2SO4 с образованием карминно-красной окраски.
А. — промежут. продукты в производстве красителей, в частности 2-А. и 4-А. — азиновых, 4-А. — тиоиндигоидных, диазолей для крашения хлопка. 4-А. — краситель для меха; в смеси с анилином используется в производстве красителя анилинового черного. Его N-алкил- и N-фенилпроизводные, напр. М-изопропил-4-А. (т. пл. 80,5 °C; трудно раств. в воде), N-фенил-4-А. (диафен; т. пл. 152 °C, раств. в спирте, не раств. в воде),-антиоксиданты и термостабилизаторы полимеров. Дихлорцинкат диазосоли 4-А. (C6H5NHC6H4N2Cr) • 2ZnCl2 — светочу вствит. компонента диазобумаги для позитивного светокопирования.
Н. Б. Карпова
