аминонафтолсульфокислоты
АМИНОНАФТОЛСУЛЬФОКИСЛОТЫ
Практич. значение имеют лишь неск. аминонафтолмоносульфокислот C10H5(NH2)(OH)SO3H и аминонафтолдисульфокислот C10H4(NH2) (ОН) (503Н)2 — бесцветные кристаллы (см. табл.), мол. м. 239,21 и 319,24 соответственно.
Аминонафтолмоносульфоки слоты обычно плохо раств. в воде, дисульфокислоты — лучше. А. практически не раств. в органических растворителях. С едкими щелочами, содой, NH3 образуют растворимые в воде соли, причем растворимость кислых солей дисульфокислот меньше, чем самих кислот, а средних солей больше. Щелочные растворы некоторых А. флуоресцируют, напр. И-кислота и гамма-кислота — синим цветом, С-кислота — голубовато-зеленым, Аш-кислота — синеватокрасным. При действии ангидридов и хлорангидридов на А. образуются N-ацильные производные.
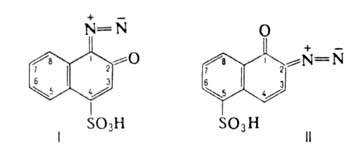
А. легко диазотируются в обычных условиях с образованием устойчивых диазосоединений. Моносульфокислоты, содержащие группы OH и NH2 в смежных положениях, диазотируются только в отсутствие минер. кислоты, но в присутствии небольшого количества соли Cu, напр. CuSO4. Таким способом в промышленности диазотируют 1-амино-2-нафтол-4-сульфокислоту с послед. использованием полученного диазосоединения (см. формулу I) в синтезе металлсодержащих азокрасителей, а также 2-амино-1-нафтол-5-сульфокислоту, диазосоединение на основе которой (формула II) используют в фоторезисторах для радиоэлектроники. Оба диазосоединения имеют строение соответствующих 1,2-нафтохинондиазидов, благодаря чему исключительно термостойки. Их можно сульфировать, нитровать, кристаллизовать из горячей воды без разложения.
1-Амино-2-нафтол-4-сульфокислота и 1-амино-8-нафтол-3,6-дисульфокислота — диазосоставляющие в синтезе азокрасителей, все остальные А. — азосоставляющие. А., у которых группы OH и NH2 находятся в разных циклах нафталинового ядра, активно вступают в азосочетание с диазосоединениями, причем азогруппа направляется в орто-положение к группе NH2 в кислой среде, к группе OH — в щелочной. Поэтому в зависимости от использованной реакц. среды можно получать два ряда моноазокрасителей, различающихся по цвету. Как правило, А. сочетают дважды (сначала в кислой среде, в которой ориентирующее действие оказывает группа NH2, а затем в щелочной) и синтезируют ценные дисазокрасители. Во всех случаях азогруппа в образующихся азосоединениях находится в орто-положеыии к группе OH или NH2, вследствие чего возможно образование комплексов с металлами. Поэтому такие азосоединения ценные протравные красители для шерсти. Кроме того, азосоединения, получаемые из 2-амино-5-нафтол-7-сульфокислоты, обладают большим сродством к непротравленному хлопку. Это свойство усиливается у ее N-ацилпроизводных.
N-Замещенные 1-амино-8-нафтол-3,6- и 1-амино-8-нафтол-4,6-дисульфокислот также широко применяют в производстве моноазокрасителей, получаемых азосочетанием в щелочной среде. N-Алкил- и N-арилпроизводные многих А. производят в пром. масштабе. Например, при нагр. 2-амино-5-нафтол-7-сульфокислоты с анилином получают N-фенилпроизводные кислоты, при ацилировании фосгеном — алую кислоту:
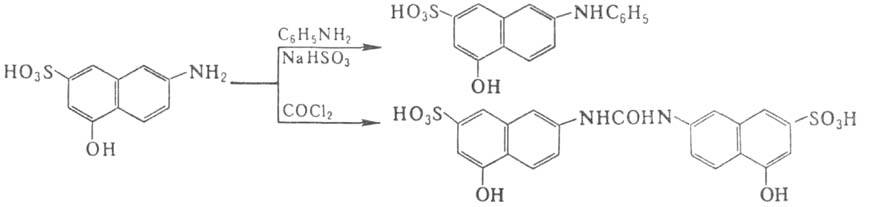
Красители из этих соед. по оттенкам и др. свойствам отличаются от азокрасителей из соответствующих незамещенных кислот.
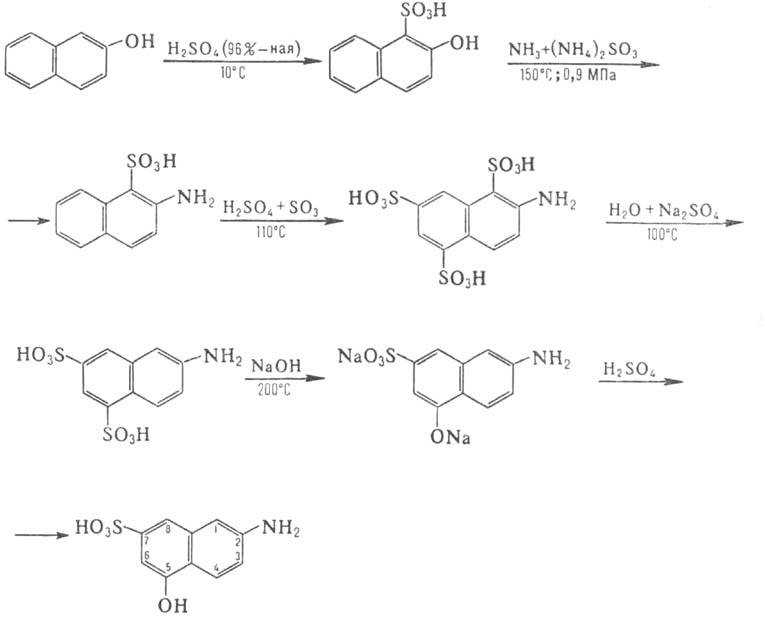
Производство любой А. — сложный многостадийный процесс. В качестве примера выше приведена схема синтеза моносульфокислоты.
ПРАКТИЧЕСКИ ВАЖНЫЕ АМИНОНАФТОЛСУЛЬФОКИСЛОТЫ

А. идентифицируют по окрашиванию водных растворов их солей под действием РеCl3. Главные методы количеств. определения-диазотирование, сочетание с диазотированными аминами в кислой и щелочной средах.
Лит.: Доналдсон Н., Химия и технология соединений нафталинового ряда, пер. с англ. М., 1963; Ч екал ин М. А., Пассет Б. В., Иоффе Б. А., Технология органических красителей и промежуточных продуктов, 2 изд., М., 1980; Эфрос Л. С., Горелик М. В., Химия и технология промежуточных продуктов, Л., 1980; Лебедев Н. Н., Химия и технология основного органического и нефтехимического синтеза, 3 изд., М., 1981.
Г. И. Пуца
