ареновые комплексы переходных металлов
АРЕНОВЫЕ КОМПЛЕКСЫ ПЕРЕХОДНЫХ МЕТАЛЛОВ
π-комплексы, содержащие одно или два ароматич. кольца (Арен) в качестве нейтральных шестиэлектронных донорных лигандов, занимающих по 3 координац. места. Известны для всех переходных металлов IV-VIII групп. Существуют гомолигандные диареновые соед. (формула I) и многочисленные гетеролигандные моноареновые соед. (напр., формулы II), в т. ч. сэндвичевые (напр., формулы III Известны также: [Арен V(CO)4]+ PF6−, [(Арен)2 МР(CH3)3] (М = Zr, Hf), мостиковые димерные соед. [Арен МCl2]2 (М = Ru, Os) и др. Ареновыми лигандами служат бензол и его производные, полиядерные ароматич. соединения. При координации с металлом ароматич. кольца почти всегда сохраняют плоское строение.
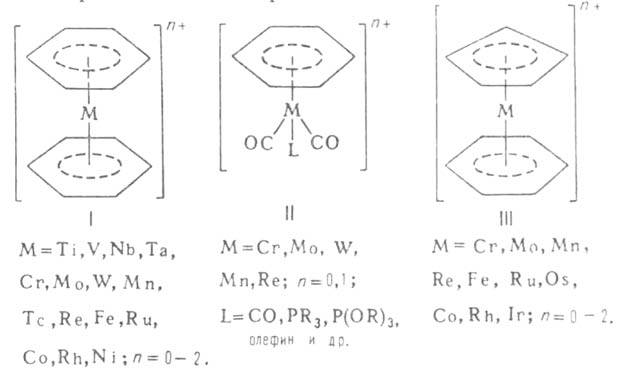
А. к. п. м., как правило, кристаллич. вещества. Их термич. разложение приводит к отщеплению лигандов и образованию металлич. "зеркала". Реакции А.к.п.м. могут быть связаны с превращениями центр. атома металла или лигандов. Первые представлены гл. обр. окислит.-восстанови г. процессами и свойственны преим. диареновым комплексам, напр.:
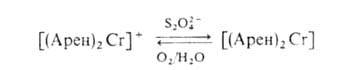
Известны случаи протонирования по металлу, напр.:
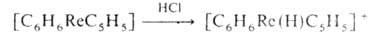
Для большинства А. к. п. м. характерен обмен лигандов, в т. ч. ареновых:
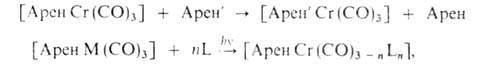
где M = Cr, Mo, W; L = RNH2, RCN, R3P, олефины и др. Реакции замещения в ареновом лиганде особенно свойственны комплексам [Арен Cr(CO)3], для которых описаны: электроф. замещение водорода (меркурирование, ацилирование, дейтерирование в кислой среде); металлированне (с помощью C4H9Li); нуклеоф. замещение галогена: [(HalC6H5)Cr(CO)3] + MX → [(XC6H5)Cr(CO)3] + MHal, где Hal = Cl, F; X = RNH, R2N, RO; М = Н, Na. Диареновые комплексы в условиях электроф. замещения окисляются, а их катионы в эти реакции не вступают. Для [(Арен)2 Cr] описано металлиро вание (с помощью C4H9Li или C5HnNa) и протофильный дейтерообмен. Катионы [(Арен)2Cr] + тоже претерпевают протофильный дейтерообмен и нуклеоф. замещение галогена. Описано электроф. ацилирование [C6H6ReC5H5] (с помощью CH3COCl/AlCl3) в оба лиганда. Комплексы [АренРеC5H4На1]+BF4 легко обменивают галогены как в шести-, так и в пятичленном лиганде на нуклеоф. группы (NH2, RO, RS, CN и др.). Специфическая реакция ареновых катионных комплексов — нуклеоф. присоединение к ареновому лиганду, напр.:
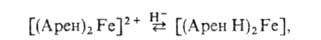
где Арен Н — неплоский циклогексадиенильный лиганд. Реакции функц. групп в координированном ареновом кольце аналогичны реакциям соответствующих заместителей в своб. аренах.
Комплексы типа [(Арен)2 М]n+, где М = V, Cr, Mo, W, Тс, Re, Fe, Ru, Co, Rh, Ni, получают обычно методом Фишера, т. е. взаимод. соли переходного металла с ареном в присутствии восстановителя (А1-пыль) и катализатора (AlCl3, А1Br3), напр.:
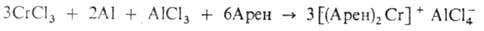
Жесткие условия этой реакции и агрессивность А1На13 позволяют использовать ее практически только для ароматических углеводородов, но и в этом случае наблюдаются побочные процессы. Все большее значение приобретает синтез [(Арен)2М] соконденсадией паров металлов и аренов. Метод требует дорогой аппаратуры, но не имеет таких ограничений, как метод Фишера. Им получены недоступные иным путем диареновые производные Ti, Zr, Hf, Nb и Та. Подавляющее большинство аренкарбонильных, часть аренциклопентадиенильных и др. гетеролигандных комплексов получают обменом лигандов:
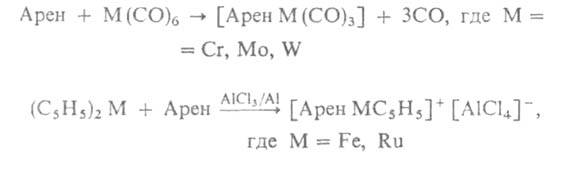
А. к. п. м. применяют для нанесения металлич. покрытий (пиролизом в вакууме) и для получения особо чистых металлов, а также как катализаторы полимеризации олефинов и диолефинов.
Лит.: Волькенау Н.А., в кн.: Методы элемснтоорганической химии. Комплексы переходных металлов с диенами, аренами, соединениями с ст-связью М—С. М., 1976, с. 127–228.
Комплексы переходных металлов с диенами, аренами, соединениями с ст-связью М—С. М., 1976, с. 127–228.
Н. А. Волькенау
