бария хлорид
БАРИЯ ХЛОРИД BaCl2
бесцветные кристаллы. До 925 °C устойчива а-модификация с ромбич. решеткой (а = = 0,7823 нм, b = 0,9333 нм, с = 0,4705 нм, пространственная группа Рпта), при 925–961 °C — β-модификация с кубич. решеткой (пространств, группа Fm3m); 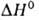 перехода
перехода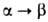 17,36 кДж/моль. Т. пл. 961 °C, т. кип. 2047 °C; плотн. 3,856 г/см3; C0p 75,14 Дж/(моль∙К);
17,36 кДж/моль. Т. пл. 961 °C, т. кип. 2047 °C; плотн. 3,856 г/см3; C0p 75,14 Дж/(моль∙К); 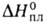 15,9 кДж/моль,
15,9 кДж/моль, 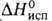 241,4 кДж/моль,
241,4 кДж/моль, 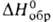 −844,0 кДж/моль,
−844,0 кДж/моль, 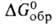 −795,8 кДж/моль; 5^8 123,7 Дж/(моль∙К). Диамагнитен. Растворимость в воде (г в 100 г): 31,7 (0 °C), 36,2 (20 °C), 58,7 (100 °C). Немного раств. в спирте, не раств. в эфире. С AlCl3, LiCl, NaCl, BaSO4, ВаTiO3, BaWO4 образует эвтектич. смеси, с ВаВг — непрерывный ряд твердых растворов, с некоторыми солями — соединения, напр. CaCl2*BaCl2, 2KCl*BaCl2, 2CsCl*BaCl2. Из водных растворов кристаллизуется ди-гидрат — бесцветные кристаллы с моноклинной решеткой (а = = 0,7136 нм, b = 0,1086 нм, с = 0,6738 нм,
−795,8 кДж/моль; 5^8 123,7 Дж/(моль∙К). Диамагнитен. Растворимость в воде (г в 100 г): 31,7 (0 °C), 36,2 (20 °C), 58,7 (100 °C). Немного раств. в спирте, не раств. в эфире. С AlCl3, LiCl, NaCl, BaSO4, ВаTiO3, BaWO4 образует эвтектич. смеси, с ВаВг — непрерывный ряд твердых растворов, с некоторыми солями — соединения, напр. CaCl2*BaCl2, 2KCl*BaCl2, 2CsCl*BaCl2. Из водных растворов кристаллизуется ди-гидрат — бесцветные кристаллы с моноклинной решеткой (а = = 0,7136 нм, b = 0,1086 нм, с = 0,6738 нм, 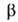 =91,08°, z = 4, пространственная группа Р21/п); плотн. 3,097 г/см3;
=91,08°, z = 4, пространственная группа Р21/п); плотн. 3,097 г/см3; 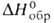 −1446,4 кДж/моль; при 100 °C обезвоживается. Известен также моногидрат — бесцветные кристаллы с ромбич. решеткой (пространств, группа Ртсп).
−1446,4 кДж/моль; при 100 °C обезвоживается. Известен также моногидрат — бесцветные кристаллы с ромбич. решеткой (пространств, группа Ртсп).
Получают Б. х.: прокаливанием смеси баритового концентрата с коксом и CaCl2 при 900–1000 °C (BaSO4 + 4C + CaCl2 → BaCl2 + CaS + 4CO); взаимод. BaS с соляной кислотой, раствором NaCl в соляной кислоте, водными растворами MgCl2, NH4C1, C12; p-цией BaC2, BaCO3, Ba(OH)2 или Ва(OOCCH3)2 с соляной кислотой. Б. х. — применяют в производстве пигментов (напр., баритового желтого BaCrO4, касселевой зелени ВаMnO4), др. соед. Ва, в качестве добавки в электролиты при получении Mg, для закалки быстрорежущей стали (в виде расплавов смеси BaCl2 с хлоридами щелочных и щел.-зем. металлов), как компонент керамики, реактив на ион SO42−, для утяжеления и осветления кожи в кожевенной промышленности, как зооцид. Б.х. токсичен; ПДК 0,5 мг/м3.
Лит. см. при статьях барий, бария гидроксид.
Т. Г. Ахштов
Значения в других словарях
- Бария хлорид — Хлористый барий, BaCl2, соль, при обычных условиях существует в виде бесцветных кристаллов дигидрата BaCl2 ․ 2H2O с плотностью 3,1 г/см3. При нагревании до 100°С теряет воду. Безводный Б. х. плавится при 960°С. Большая советская энциклопедия
