бензилцианид
БЕНЗИЛЦИАНИД (нитрил фенилуксусной кислоты, фенилацетонитрил, α-циантолуол) C6H5CH2CN
мол. м. 117,15; бесцветная жидкость с ароматич. запахом; т. пл. −23,8 °C, т. кип. 233,9±0,2 °C, 107 °C/12 мм рт. ст.; d420 1,018; nD201,5242; температурная зависимость давления пара (в мм рт. ст.) в интервале 333–508 К выражается уравнением: lg p (мм)= 8,4130–2794,6/T; η 1,97 мПа∙с (25 °C); γ 41,4 мН/м (20 °C), 36,75 мН/м (60 °C); μ 1,16∙10−29 Кл∙м (бензол; 25 °C); ε 18,7 (27 °C); 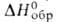 −194,4 кДж/моль,
−194,4 кДж/моль, 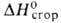 — 4,28 МДж/моль; не раств. в воде, смешивается во всех соотношениях со спиртом и эфиром, хорошо раств. в других органических растворителях. Вследствие наличия активной метиленовой группы Б. — CH-кислота (pKа 21,3; ДМСО), образует соли со щелочными металлами, напр. C6H5CH(Na)CN и C6H5C(Na)2CN, взаимод. с карбонильными соед. (реакция Кнёвенагеля):
— 4,28 МДж/моль; не раств. в воде, смешивается во всех соотношениях со спиртом и эфиром, хорошо раств. в других органических растворителях. Вследствие наличия активной метиленовой группы Б. — CH-кислота (pKа 21,3; ДМСО), образует соли со щелочными металлами, напр. C6H5CH(Na)CN и C6H5C(Na)2CN, взаимод. с карбонильными соед. (реакция Кнёвенагеля):
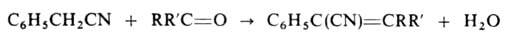
Для Б. также характерны реакции с участием бензольного кольца и цианогруппы (см. нитрилы). В промышленности Б. обычно получают реакцией бензилхлорида с небольшим избытком NaCN или KCN в водно-спиртовой среде при 75–85 °C Добавки третичных аминов, Nal или KI ускоряют реакцию. Из реакционной смеси Б. выделяют ректификацией; выход 80–85%. С использованием катализаторов межфазного переноса, напр. бензилтриэтиламмоний-хлорида, выход возрастает до 94%. Б. также м. б. получен окислительным аммонолизом этилбензола при 200–450 °C (кат. — смесь оксидов V, Sb и U или Cr): C6H5CH2CH3 + NH3 + 1,5O2 → C6H5CH2CN + 3H2O и взаимод. толуола с ClCN при 550–800 °C: C6H5CH3 +ClCN → C6H5CH2CN + HCl.
Б. — сырье в производстве фенилуксусной кислоты и ее производных, пестицида фоксима (валексона), лек. веществ (дибазол, фенакон, фенамин) и бромбензилцианида. Для Б. т. всп. 106 °C, т. воспл. 115 °C, т. самовоспл. 498 °C; температурные пределы воспламенения 55–139 °C. Обладает местным раздражающим действием, проникает через неповрежденную кожу; ПДК 0,8 мг/м3; ЛД50 78 мг/кг и 270 мг/кг (перорально; соотв. мыши и крысы). Впервые Б. получен С. Канниццаро в 1855 взаимод. бензилхлорида с KCN.
Лит.: ЗильберманЕ.Н., Реакции нитрилов, М., 1972.
С. К. Смирнов
