бензохиноны
БЕНЗОХИНОНЫ
мол. м. 108,10. Существуют в виде двух изомеров-1,2- и 1,4-Б. (формулы соотв. I и II).
1,2-Б. (3,5-циклогексадиен-1,2-дион; о-бензохинон; о-хинон) — ярко-красные кристаллы; т. разл. 70–80 °C, окислительно-восстановит. потенциал Е° — 0,795 В (H20; 25 °C); μ 17,03∙10−30 Кл∙м (бензол; 20 °C); раств. в воде, спирте, легко — в эфире, гексане, хлороформе; в растворах неустойчив.
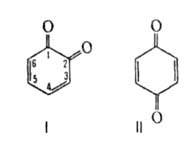
1,4-Б. (2,5-циклогексадиен-1,4-дион; n-бензохинон; хинон) — золотисто-желтые кристаллы с резким запахом; т. пл. 116 °C; d4201,320; легко возгоняется; перегоняется с паром; μ 2,51∙10−30 Кл∙м (бензол; 20 °C); 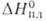 20,95 кДж/моль;
20,95 кДж/моль; 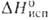 47,76 кДж/моль (115–128 °C); S0298 −187,5 кДж/моль; окислительно-восстановительный потенциал Е° — 0,711 В (бензол; 25 °C);
47,76 кДж/моль (115–128 °C); S0298 −187,5 кДж/моль; окислительно-восстановительный потенциал Е° — 0,711 В (бензол; 25 °C); 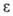 3,12 (17 °C); легко растворим в спирте, эфире, горячем лигррине; растворимость в воде 0,7% (5 °C1 1,5% (30 °C).
3,12 (17 °C); легко растворим в спирте, эфире, горячем лигррине; растворимость в воде 0,7% (5 °C1 1,5% (30 °C).
Б. легко и обратимо восстанавливаются H2 (кат. — РЮ2), SO2, гидразином, напр.:
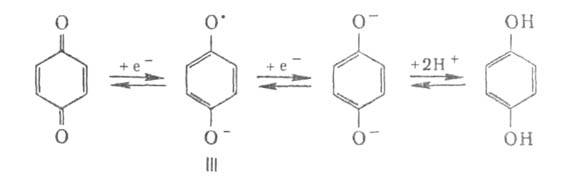
Благодаря способности превращаться в устойчивые анионрадикалы — семихиноны (III) Б. образуют с донорами электронов прочные комплексы с переносом заряда, напр. 1,4-Б. — с бензолом, толуолом, нафталином, антраценом в соотношении 1:1, с фенолом — 1:1 и 1:2 (фенохинон), гидрохиноном — 1:1 (хингидрон). Последний — темно-фиолетовые кристаллы с металлич. блеском; т. пл. 171 °C; μ 6,68∙10−30 Кл∙м (диоксан; 20 °C); 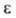 4,12 (17 °C); окислительно-восстановит. потенциал Е° 0,699 В (вода; 25 °C); растворимость в воде 0,35% (20 °C), 1,035% (50 °C); распадается на компоненты в растворе уксусной кислоты. Действием порошка Zn в уксусном ангидриде Б. превращ. в диацетоксибензолы.
4,12 (17 °C); окислительно-восстановит. потенциал Е° 0,699 В (вода; 25 °C); растворимость в воде 0,35% (20 °C), 1,035% (50 °C); распадается на компоненты в растворе уксусной кислоты. Действием порошка Zn в уксусном ангидриде Б. превращ. в диацетоксибензолы.
1,4-Б. с первичными аминами образует замещенные монохинонимины (IV), с гидроксиламином-n-хинонмонооксим (таутомерен с n-нитрозофенолом) и n-хинондиоксим (V). 1,2-Б. с о-фенилендиамином дает феназин (VI).
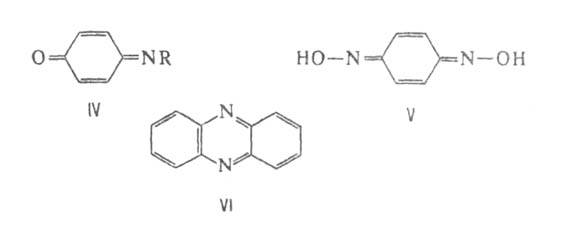
При взаимодействии с реактивом Гриньяра Б. превращ. в хинолы (VII), перегруппировывающиеся в алкилгидрохиноны, напр.:
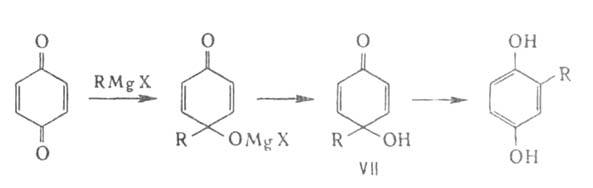
Б., подобно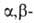 ненасыщенным кетонам, способны к 1,2-присоединению по связи C—C и 1,4-присоединению по связям C=C и C=O. Продукты 1,4-присоединения окисляются избытком исходного Б., если их окислительно-восстановит. потенциал ниже, чем у Б. Так, с метанолом 1,4-Б. образует 2,5-диметокси-1,4-бензохинон (кат. — ZnCl2), с анилином — 2,5-дианилино-1,4-бензохинон. В реакции Дильса — Альдера 1,2-Б. выступает как диен и диенофил, 1,4-Б. — как диенофил. Так, 1,4-толухинон с 1,3-бутадиеном в бензоле на холоду образует 2-метил-5,8,9,10-тетрагидронафтохинон (VIII), который дегидрируется при 120 °C в 2-метил-1,4-нафтохинон (витамин K3):
ненасыщенным кетонам, способны к 1,2-присоединению по связи C—C и 1,4-присоединению по связям C=C и C=O. Продукты 1,4-присоединения окисляются избытком исходного Б., если их окислительно-восстановит. потенциал ниже, чем у Б. Так, с метанолом 1,4-Б. образует 2,5-диметокси-1,4-бензохинон (кат. — ZnCl2), с анилином — 2,5-дианилино-1,4-бензохинон. В реакции Дильса — Альдера 1,2-Б. выступает как диен и диенофил, 1,4-Б. — как диенофил. Так, 1,4-толухинон с 1,3-бутадиеном в бензоле на холоду образует 2-метил-5,8,9,10-тетрагидронафтохинон (VIII), который дегидрируется при 120 °C в 2-метил-1,4-нафтохинон (витамин K3):
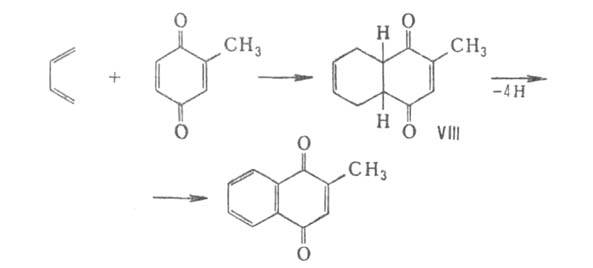
С H2O2 в щелочной среде Б. образует эпоксигидрохинон, превращающийся в кислой среде в гидроксихинон, напр.:
Атомы Н ядра Б. способны замещаться, напр. с фенилдиазонийхлоридом 1,4-Б. образует 2-фенил-1,4-бензохинон, 1,2-Б.-4-фенил-1,2-бензохинон (реакция Меервейна).
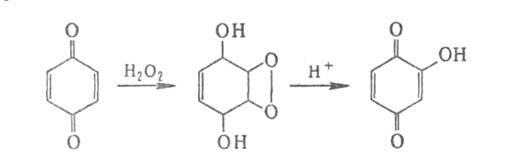
1,2-Б. действием O2 (кат. — комплекс CuCl2-пиридин) в среде метанола расщепляется с образованием моно- и диметилмуконатов:
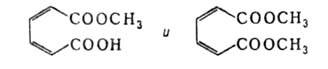
1,4-Б. устойчив к действию окислителей.
Гидроксибензохинон существует в двух таутомерных формах:
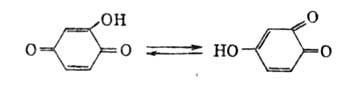
Они этерифицируются при нагр. в спирте в присутствии кислых катализаторов. Галоген- и алкоксибензохиноны легко омыляются щелочными агентами до гидроксибензохинонов. Атом галогена в галогенбензохинонах легко замещается на амино- и алкоксигруппы.
Замещенные 1,4-Б. — окислители, обратимо восстанавливающиеся в гидрохиноны. Они участвуют в переносе электронов в процессах клеточного дыхания. В промышленности 1,4-Б. получают окислением анилина действием MnO2 (пиролюзит) в H2SO4 при 3–10 °C или Na2Cr2O7 в H2SO4 при 20 °C. Аналогично из замещенных анилинов получают замещенные 1,4-Б., напр. толухинон, n-ксилохинон, 2,6-диметил-1,4-бензохинон. 1,2-Б. и его алкилпроизводные получают из соответствующих пирокатехинов окислением Ag2O в сухом эфире в присутствии Na2SO4 при 20 °C или PbO2 в бензоле в присутствии Na2SO4 (выход 70%). 1,4-Б. — промежут. продукт в производстве гидрохинона. Его применяют в производстве красителей, как дубящее вещество. Он вызывает превращ. гемоглобина в метгемоглобин, что приводит к анемии; раздражает кожу; ПДК 0,05 мг/м3. 1,4-Б. впервые получен А. А. Воскресенским в 1838 окислением хинной (тетрагидроксибензойной) кислоты MnO2 в H2S04.
Лит.: Кэсон Д., в сб.: Органические реакции, пер. с англ., сб. 4, М., 1951, с. 270–336; MortonR.A.. Biochemistry, of quinones, L. N.Y., 1965; Ullmanns Encyklopadie, Bd 8, Weinheim-N.Y., 1977, S. 364.
Н. Б. Карпова
