Брауна правило селективности
БРАУНА ПРАВИЛО СЕЛЕКТИВНОСТИ
в реакциях электроф. замещения в ароматич. ряду селективность тем выше, чем меньше кислотность реагента по Льюису.
Скорость взаимод. вещества, обладающего большим электронным дефицитом на реакц. центре (сильная кислота), а следовательно, и высокой реакц. способностью, сравнительно мало зависит от смещения электронов в бензольном кольце, вызываемом заместителем. С уменьшением кислотности реагента его реакционная способность падает, возрастает зависимость скорости реакции от смещения электронной плотности в бензольном кольце и, следовательно, от природы заместителя. В связи с этим катион Br+, генерируемый HBrO в присутствии HClO4 (сильная кислота), слабо "различает" активный толуол и менее активный бензол и бромирует толуол в пара-положение только в 36 раз быстрее. В то же время Br2 (слабая кислота) в присутствии 85% CH3COOH реагирует с толуолом в 600 раз быстрее. В этом случае говорят о межмолекулярной селективности замещения (fn), которую количественно оценивают как отношение скоростей реакций замещения в пара-положение замещенного бензола и в бензоле при действии одного и того же реагента.
Когда электрофил — сильная кислота, возможность образования разл. замещенных бензола (внутримолекулярная селективность) в определенной степени уравнивается. Это, в частности, объясняется тем, что стадией, определяющей в данном случае скорость реакции, м. б. образование комплекса I:
комплекса I:
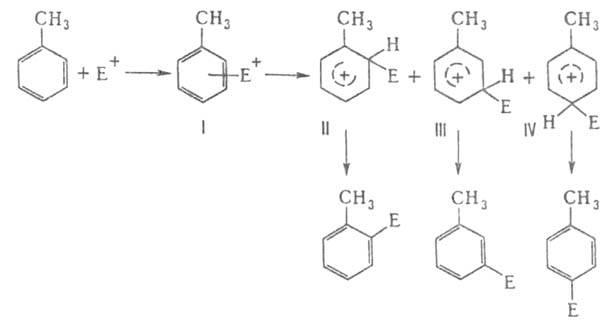
где Е+-электрофил. Если последний представляет собой слабую кислоту, лимитирующая стадия-образование комплексов II-IV. В этом случае возможна перегруппировка первоначально неселективно образующихся
комплексов II-IV. В этом случае возможна перегруппировка первоначально неселективно образующихся комплексов в более устойчивые, что обусловливает большую внутримолекулярную селективность. Так, при алкилировании толуола с помощью C3H7Вг в присутствии GaBr3 (сильная кислота) образуется 46,8% пара- и 25,7% мета-замещенных, а при бромировании с помощью Br2 в CF3COOH (слабая кислота) — соотв. 84,2% и 0%. Внутримолекулярная селективность количественно оценивается величиной fn/fm, где fm-отношение скоростей реакций замещения в .мета-положение замещенного бензола и в бензоле при действии одного и того же реагента. График зависимости lg fn от lg(fn/fm) представляет собой прямую линию и описывается уравнением:
комплексов в более устойчивые, что обусловливает большую внутримолекулярную селективность. Так, при алкилировании толуола с помощью C3H7Вг в присутствии GaBr3 (сильная кислота) образуется 46,8% пара- и 25,7% мета-замещенных, а при бромировании с помощью Br2 в CF3COOH (слабая кислота) — соотв. 84,2% и 0%. Внутримолекулярная селективность количественно оценивается величиной fn/fm, где fm-отношение скоростей реакций замещения в .мета-положение замещенного бензола и в бензоле при действии одного и того же реагента. График зависимости lg fn от lg(fn/fm) представляет собой прямую линию и описывается уравнением:
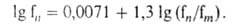
Влияние заместителей в бензольном кольце на селективность при электроф. ароматич. замещении описывается модифицир. уравнением Гаммета: 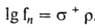 . Каждому заместителю в бензольном кольце соответствует своя константа
. Каждому заместителю в бензольном кольце соответствует своя константа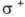 , которая характеризует его способность стабилизировать промежуточно образующийся
, которая характеризует его способность стабилизировать промежуточно образующийся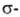 комплекс. Каждому типу реакции соответствует своя константа
комплекс. Каждому типу реакции соответствует своя константа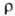 -мера близости реального промежуточного состояния в реакции к такому комплексу.
-мера близости реального промежуточного состояния в реакции к такому комплексу.
Не подчиняются Б. п. с. нитрование и арилирование толуола в среде CH3NO2 соотв. с помощью NO2BF4 и C6H5С1*AlCl3. Правило сформулировано Г. Брауном в 1953.
Лит.: Бреслоу Р., Механизмы органических реакций, пер. с англ., М., 1968, с. 168–81, 189–99; Беккер Г., Введение в электронную теорию органических реакций, пер. с нем., М., 1977, с. 521–26; Днепровский А.С, Темникова Т. И., Теоретические основы органической химии, Л., 1979, с. 377–79; Общая органическая химия. пер. с англ., т. 1, М., 1981, с. 385–86.
Н. С. Яшина
