Бухерера реакции
БУХЕРЕРА РЕАКЦИИ
1) Замещение группы OH на NH2 в ароматич. соед. (гл. обр. в нафтолах) действием NH3 и водных растворов гидросульфитов при 90–180 °C (наз. также реакцией Бухерера — Лепти), напр.:
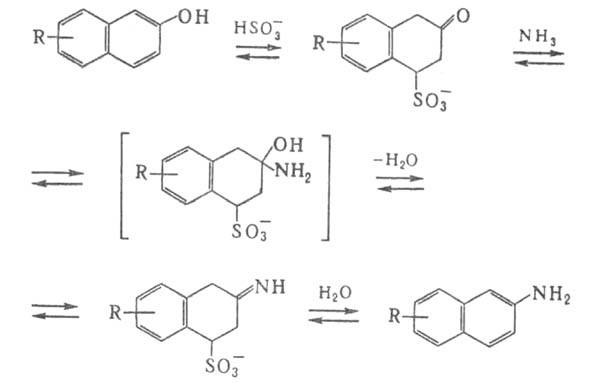
Реакция обратима: при нагр. нафтиламинов с гидросульфитами образуются нафтолы. В реакцию вступают только соед., способные к кето-енольной таутомерии, в т. ч. производные гидрохинона и резорцина.
У производных хинолина и изохинолина обмениваются группы OH (или NH2), находящиеся только в бензольном кольце. Использование в реакции с нафтолами сульфита гидразина позволяет получать нафтилгидразины. В более жестких условиях гидроксил м. б. замещен на алкиламино-или диалкиламиногруппы. Особенно реакционноспособны 1-гидроксинафталин-4-сульфокислоты; нафтолы с группами COOH или SO3H в орто- и мета-положениях в реакцию не вступают. Влияние этих заместителей используют для селективного замещения только одной из групп в диамино-или дигидооксинафталинах, напр.:
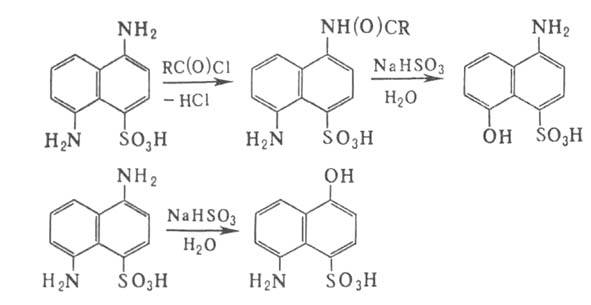
Реакцию применяют в синтезе красителей. Впервые реакция описана Р. Лепти в 1903 и развита как синтетич. метод Г. Бухерером в 1904.
Лит.: Дрейк Н., в кн.: Органические реакции, пер. с англ., сб. 1, М, 1948, с. 133–62; Ворожцов Н. Н., Основы синтеза промежуточных продуктов и красителей, М., 4 изд., 1955, с. 405.
2) Синтез бензокарбазолов взаимод. нафтолов с фенилгидразином и NaHSO3:
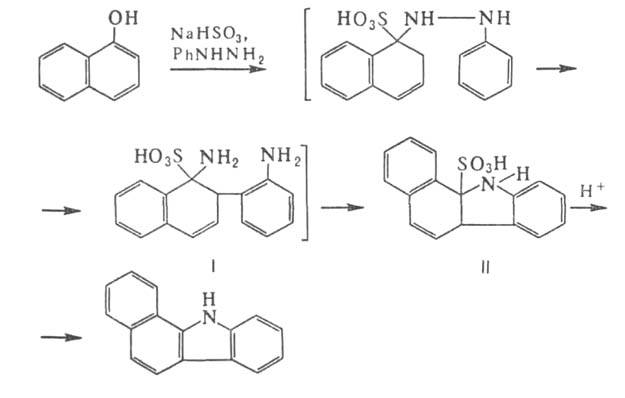
Из α-нафтолов первоначально образуется аддукт (I), из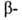 нафтолов — сразу соед. типа (II), причем в первом случае образуется 1,2-, во втором — 3,4-бензокарбазолы. Вместо нафтолов м. б. использованы нафтиламины. Аналогично фенилгидразину реагируют н-толил-, α-и
нафтолов — сразу соед. типа (II), причем в первом случае образуется 1,2-, во втором — 3,4-бензокарбазолы. Вместо нафтолов м. б. использованы нафтиламины. Аналогично фенилгидразину реагируют н-толил-, α-и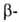 нафтилгидразины, а также N,N-дизамещенные гидразины. Реакция открыта Г. Бухерером в 1908.
нафтилгидразины, а также N,N-дизамещенные гидразины. Реакция открыта Г. Бухерером в 1908.
3) Получение 5-замещенных гидантоинов последовательной обработкой альдегидов или кетонов синильной кислотой и (NH4)2CO3 (этот синтез наз. также реакцией Бухерера — Бергса):
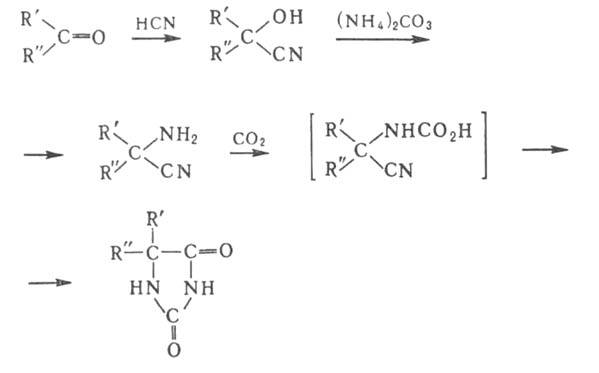
Кетоны реагируют быстрее альдегидов, вместо которых удобно использовать их гидросульфитные производные. Вместо HCN можно применять NaCN или KCN. Взаимод. кетонов или α-аминонитрилов с CS2 получают 2,4-дитиотидантоины. Реакцию применяют для идентификации карбонильных соед., а также для синтеза α-аминокислот (гидролизом гидантоинов).
Реакция открыта Г. Бергсом в 1929 и позднее подробно изучалась Г. Бухерером.
Лит.: Chubb F. [а.о.], "J. of Org. Clicm.", 1980, v. 45, № 12, p. 2315–20; SacripanteG., Edward J., "Canad. J. Chcm.", 1982, v. 60, № 15, p. 1982–87.
Д. И. Махонькое
