цианэтилирование
ЦИАНЭТИЛИРОВАНИЕ (β-цианэтилирование)
введение в молекулу β-цианэтильной группы. Осуществляется действием акрилонитрила на спирты, фенолы, тиолы и др. соед. с подвижным атомом Н в присутствии основных катализаторов (щелочи, алкоголяты и др.) в среде орг. растворителя (бензол, ацетонитрил и др.). В некоторых случаях катализаторами могут служить кислоты.
Ц. — частный случай Михаэля реакции. Ц. протекает через промежут. образование карбаниона; последний в избытке акрилонитрила способен к присоединению еще одной молекулы нитрила, напр.:
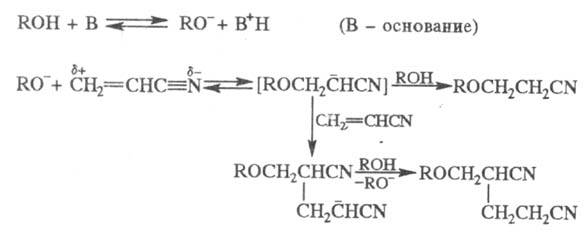
Реакция с первичными спиртами — экзотермическая, вторичные спирты реагируют труднее первичных, третичные в обычных условиях в реакцию не вступают. Подобно одноатомным спиртам реагируют гликоли и многоатомные спирты, а также этиленциангидрин, оксимы, аминоспирты. Для последних при наличии в аминогруппе свободного атома водорода реакция идет по атому азота.
Фенолы цианэтилируются по гидроксильной группе и в ядро, напр.:
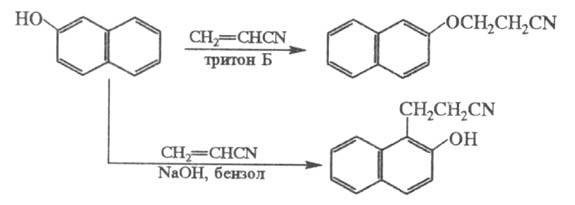
Электроотрицат. группы препятствуют реакции; так, выход продукта Ц. n-хлорфенола менее 10%.
Тиолы реагируют с ахрилонитрилом более энергично, чем спирты. Ц. алифатич. и ароматич. тиолов приводит к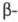 алкил(арил)тиопропионитрилам RSCH2CH2CN, Ц. гидросульфитов и сульфинатов — к производным S(VI):
алкил(арил)тиопропионитрилам RSCH2CH2CN, Ц. гидросульфитов и сульфинатов — к производным S(VI):
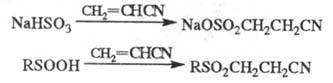
При Ц. сероводорода образуется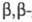 дицианодиэтилсульфид S(CH2CH2CN)2. Аналогично реагирует вода.
дицианодиэтилсульфид S(CH2CH2CN)2. Аналогично реагирует вода.
Ц. аммиака в зависимости от условий приводит к продуктам моно-, ди- и трицианэтилирования (реакция обратимая). Первичные амины цианэтилируются в отсутствие катализатора, труднее идет реакция с циклич. вторичными аминами (напр., пиперидином, морфолином) и еще труднее с ациклич. вторичными аминами. Ароматич. амины вступают в реакцию при повышенной температуре в присутствии кислот (H2SO4, ледяная CH3COOH и др.); ускоряют реакцию соли Cu, Zn, Co, Ni.
При Ц. цианамида в присутствии водной щелочи образуется продукт бисцианэтилирования, обладающий сильным инсектицидным действием:
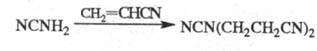
Циклич. амиды, особенно имиды, в присутствии щелочей довольно легко цианэтилируются по иминогруппе:
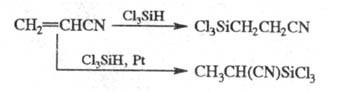
В присут. оснований силаны реагируют с акрилонитрилом по механизму цианэтилирования; в присутствии Pt направление реакции меняется:
цианэтилирования; в присутствии Pt направление реакции меняется:
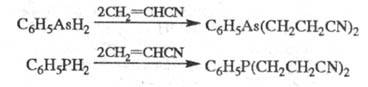
Незамещ. фосфин цианэтилируется, подобно аммиаку, Ц. первичных фосфинов и арсинов приводит к бис-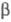 -цианэтилзамещенным соед.:
-цианэтилзамещенным соед.:
Гладко идет Ц. галогеноводородов с образованием HalCH2CH2CN, синильной кислоты — с образованием сукцинонитрила NCCH2CH2CN.
Ц. применяют в промышленности для получения сукцинонитрила, а также для модификации свойств некоторых полимеров (крахмала, целлюлозы и др.).
Лит.: Терентьев А.П., Кост А.Н., в кн.: Реакции и методы исследования органических соединений, кн. 2, М- Л., 1952, с. 47–208; Kirk-Othmer encyclopedia, 3 ed., v. 7, N. Y., 1979, p. 370–85.
С. К. Смирнов, С. С. Смирнов
