циклододекан
ЦИКЛОДОДЕКАН (додекаметилен)
мол. м. 168,32; прозрачные бесцветные кристаллы; т. пл. 61–63 °C, т. кип. 243 С, 118 °C/18 мм рт. ст.; 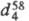 0,8340;
0,8340; 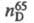 1,4550;
1,4550; 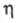 2,0 мПа∙с (70 °C);
2,0 мПа∙с (70 °C); 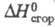 −660,3 кДж/моль (в расчете на группу CH2),
−660,3 кДж/моль (в расчете на группу CH2), 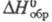 −60 кДж/моль. Не раств. в воде, раств. в диэтиловом эфире, бензоле. Молекула Ц. неплоская, наиб. вероятная, энергетически выгодная конформация — деформир. "корона". Кристаллич. решетка триклинная (а — 0,784 нм, b = 0,544 нм, с = 0,782 нм, α= 8Г42', β= 64°,
−60 кДж/моль. Не раств. в воде, раств. в диэтиловом эфире, бензоле. Молекула Ц. неплоская, наиб. вероятная, энергетически выгодная конформация — деформир. "корона". Кристаллич. решетка триклинная (а — 0,784 нм, b = 0,544 нм, с = 0,782 нм, α= 8Г42', β= 64°, 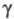 = 81°, Z=l).
= 81°, Z=l).
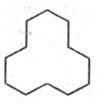
Ц. относится к слабонапряженным карбоциклич. соед. (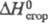 в расчете на группу CH2 лишь на 1,3 кДж/моль выше, чем у алканов). Напряжение молекулы Ц. обусловлено гл. обр. деформацией валентных углов (некоторые углы ССС в Ц. достигают 117° против нормального значения 109o28'). Меньший вклад в общее напряжение вносят прелоговское и питцеровское напряжения (см. напряжение молекул).
в расчете на группу CH2 лишь на 1,3 кДж/моль выше, чем у алканов). Напряжение молекулы Ц. обусловлено гл. обр. деформацией валентных углов (некоторые углы ССС в Ц. достигают 117° против нормального значения 109o28'). Меньший вклад в общее напряжение вносят прелоговское и питцеровское напряжения (см. напряжение молекул).
Ц. — относительно устойчивое соед. Взаимод. с галогенами приводит к последоват. замещению атомов Н на галоген. Ц. не реагирует с галогеноводородными кислотами даже при натр. до 250 °C. При действии H2 в присуг. Pt или Ni изомеризуется с сужением цикла. Такая же изомеризация происходит в присуг. AlCl3 или под воздействием высоких температур. При окислении Ц. KMnO4 либо минеральными кислотами образуется 1,10-декандикарбоновая кислота, при окислении O2 воздуха в жидкой фазе в присутствии переходных металлов или соед. бора — смесь продуктов с преимущественным содержанием циклододеканола. Последний через ряд последоват. реакций (дегидрирование на меднохромовом кат. и послед. превращение продукта реакции в оксим, перегруппировка Бекмана в присутствии конц. H2SO4, гидролитич. полимеризация) превращается в полидодеканамид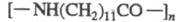 — термопласт (мол. м. 15 000–35 000, т. пл. 178–180 °C,
— термопласт (мол. м. 15 000–35 000, т. пл. 178–180 °C, 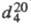 1,02; не раств. в воде, низших спиртах, муравьиной кислоте, устойчив в маслах, жирах, разбавленных кислотах и растворах щелочей).
1,02; не раств. в воде, низших спиртах, муравьиной кислоте, устойчив в маслах, жирах, разбавленных кислотах и растворах щелочей).
В промышленности Ц. получают с количеств. выходом гидрированием цис,транс,транс- или транс,транс,транс- 1,5,9-циклододекатриенов (продуктов циклотримеризации бутадиена) в присутствии Ni, Co, Cu, Pd или др. катализаторов на носителях (Al2O3, SiO2, уголь) при 20–25 °C и давлении 1–30 МПа.
Известен способ получения Ц. гидрированием на гетерогенных катализаторах углеводородной фракции C4 пиролиза нефтепродуктов, содержащей 35–40% (по массе) бутадиена.
Ц. — полупродукт для получения полидодеканамида (компонент антифрикционных, конструкционных и электроизоляционных изделий, напр. вкладышей подшипников, деталей точных измерит. приборов), 1,10-декандикарбоновой кислоты (сырье для получения полиамидных волокон типа модифицир. найлона, смазок, пластификаторов), а также для получения циклододеканола и циклододеканона.
Ц. пожароопасен, т. всп. 95 °C, т. воспл. 105 °C, т. самовоспл. 350 С.
Лит.: Илиел Э., Стереохимия соединений углерода, пер. с англ., М., 1965; Справочник нефтехимика, под ред. С. К. Огородником, т. 1, Л., 1978, с. 18.
В. Я. Кугель
