циркония сплавы
ЦИРКОНИЯ СПЛАВЫ
Осн. легирующие элементы — Sn, Cr, Nb, Cu и Mo, содержание которых не более 1,5–2,5%; в отдельных Ц. с. в небольших количествах присутствуют Fe и Ni, которые как примеси при выплавке циркония попадают из цирконовой губки. Ц. с. характеризуются высокой кратковременной прочностью (300–450 МПа, 300 °C), высоким сопротивлением ползучести (при 350 °C и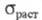 200 МПа скорость ползучести
200 МПа скорость ползучести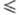 0,4∙10−4 %/ч), коррозионной стойкостью при 300–350 °C на воздухе, в O2, CO2, H2O и водяном паре, орг. и жидкометаллич. (Na, К, Pb и др.) теплоносителях; по некоторым теплофиз. свойствам (тепло- и температуропроводность, термич. коэф. линейного расширения и др.) превосходят аустенитные нержавеющие стали. Обладают высокой радиац. стойкостью, низким поперечным сечением захвата тепловых нейтронов (~ 0,18∙10−28м2); совместимы (не взаимодействуют) с ядерным горючим (U, его сплавы с Mo, Nb и Zr, а также UO2, UC, U3Si и др.).
0,4∙10−4 %/ч), коррозионной стойкостью при 300–350 °C на воздухе, в O2, CO2, H2O и водяном паре, орг. и жидкометаллич. (Na, К, Pb и др.) теплоносителях; по некоторым теплофиз. свойствам (тепло- и температуропроводность, термич. коэф. линейного расширения и др.) превосходят аустенитные нержавеющие стали. Обладают высокой радиац. стойкостью, низким поперечным сечением захвата тепловых нейтронов (~ 0,18∙10−28м2); совместимы (не взаимодействуют) с ядерным горючим (U, его сплавы с Mo, Nb и Zr, а также UO2, UC, U3Si и др.).
Основа Ц. с. — твердый раствор легирующих элементов в α-мо-дификации Zr с гексаген. кристаллической решеткой, устойчивой до 863 °C. Примеси, образующие твердые растворы внедрения (N, О, С и Н), отрицательно влияют на технол. свойства (обрабатываемость давлением), коррозионную стойкость и эксплуатац. свойства Ц. с.; содержание их ограничивают жесткими пределами (напр., содержание N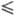 0,006–0,008%). В отдельных Ц. с. допускают присутствие 0,1–0,15% О, который можно считать легирующим элементом, упрочняющим α-Zr.
0,006–0,008%). В отдельных Ц. с. допускают присутствие 0,1–0,15% О, который можно считать легирующим элементом, упрочняющим α-Zr.
Среди Ц. с. наиб. известны циркаллои (1,2–1,7% Sn, 0,05–0,15% Cr, 0,07–0,24% Fe, 0,007–0,08% Ni), оженит (0,25% Sn, по 0,1% Cr, Fe и Ni), а также сплавы Zr — 1% Nb и Zr — 2,5% Nb. Слитки Ц. с. выплавляют в вакуумных злектродуговых и электроннолучевых печах; полуфабрикаты и изделия (трубы, прутки, листы, проволока) получают из слитков методами горячей и холодной деформации с промежут. отжигами.
Ц. с. типа циркаллои используют в холоднодеформированном, частично или полностью рекристаллизованном состоянии. Отдельные Ц. с. [Zr-Nb (2,5%), Zr-Cr (1,2%) — Fe (0,1%) и др.] для повышения прочности и сопротивления ползучести подвергают закалке и отпуску.
В процессе работы Ц. с. взаимод. с H2O и водяным паром, что приводит к их наводороживанию с образованием ZrH2; при этом повышается прочность сплавов и снижается пластичность (на 70–80%). Наиб. изменение мех. свойств наблюдается при увеличении концентрации H2 до ~ 0,08%.
Мех. свойства Ц. с. изменяются также под действием нейтронного облучения; при этом происходят снижение пластичности на 35–40% и рост предела текучести при растяжении (остаточная деформация 0,2%) на 50–100%. Макс. значение предела текучести, близкое к значениям кратковременной прочности, наблюдается при облучении потоком нейтронов плотностью 1021 см−2. Нейтронное облучение увеличивает скорость ползучести и резко снижает ударную вязкость Ц. с., повышая их температуру перехода из пластичного в хрупкое состояние, особенно при небольших концентрациях H2. Так, при содержании в сплаве 0,002% Н облучение повышает температуру перехода на 100–200 °C, а при 0,02% Н — на 50–200 °C; при этом критич. температура хрупкости может оказаться на уровне рабочих температур Ц. с. в ядерных реакторах (300–350 °C).
Ц. с — конструкц. материалы активной зоны ядерных реакторов; из них изготавливают оболочки твэлов (срок службы от 1,5 до 6 лет), детали тепловыделяющих сборок и технол. каналы (срок службы до ~ 30 лет) энергетич. ядерных реакторов на тепловых нейтронах с пароводяным теплоносителем. Ц. с. можно использовать в активной зоне ядерных реакторов на тепловых и быстрых нейтронах с жидкометаллич. или углекислотным теплоносителем, работающих при температурах 500–550 °C, а также как матрицу для диспергирования соед. U в сердечниках дисперсионных твэлов.
Лит.: Займовский А.С., Калашников В.В., Головин И. С., Тепловьщеляющие элементы атомных реакторов, М., 1966; Ривкин Е. Ю., Родченков Б. С, Филатов В. М., Прочность сплавов циркония, М., 1974; Займовский А. С., Никулина А.В., Решетников Н.Г., Циркониевые сплавы в атомной энергетике, М., 1981.
А. М. Захаров
