флуорантен
ФЛУОРАНТЕН
мол. м. 202,26; бесцветные кристаллы, т. пл. 110,4–111,4 °C,т. кип. 382–383 °C, 217 °C/30 мм рт. ст.; 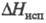 329 кДж/кг,
329 кДж/кг, 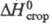 −39130 кДж/кг (25 °C). Не раств. в воде, легко раств. в диэтиловом эфире, горячем этаноле.
−39130 кДж/кг (25 °C). Не раств. в воде, легко раств. в диэтиловом эфире, горячем этаноле.
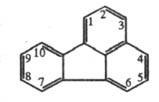
Восстановление Ф. Na в спирте приводит к 1,2,3,10b-тетрагидрофлуорантену, гидрирование в присутствии Ni — к пергидро-флуорантену. Ф. окисляется хромовой кислотой сначала до флуорантен-2, 3-хинона, а затем до 9-флуоренон-1-карбоновой кислоты. При электроф. замещении активны положения 3 и 8. При фотохим. бромировании в CS2 образуются 3- и 8-бром-производные, в CH3COOH — 3,8,9-трибромфлуорантен, при нитровании HNO3 в CH3COOH — смесь 3- и 8-нитропроиз-водных. Сульфирование конц. H2SO4 приводит к флуоран-тен-3,9-дисульфокислоте, которая при сплавлении с KOH превращается в 3,9-дигидроксифлуорантен. Ф. вступает в реакции Фриделя — Крафтса: взаимод. с CH3COCl дает смесь 3- и 8-ацетилфлуорантенов с 3,9-диацетилпроизводным, взаимод. с бензоилхлоридом — 8-бензоилфлуорантен с примесью 4-бензоилфлуорантена, с фталевым ангидридом в CS2 в присутствии AlCl3 образуется смесь 2-(3-флуорантеноил)- и 2-(8-флуо-рантеноил)бензойных кислот.
Ф. в количестве 2–3,5% содержится во фракции "антраценовое масло" кам.-уг. смолы.
В промышленности Ф. получают перегонкой кам.-уг. смолы; очищают перекристаллизацией. Препаративно синтезируют по схеме:
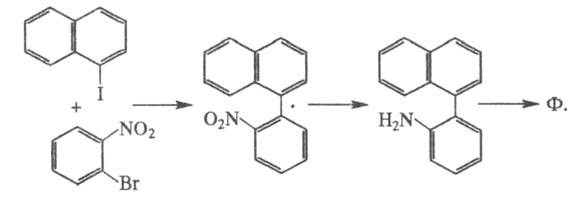
Применяют Ф. для получения флуоресцентных красителей; тетрагидропроизводные Ф. — исходные продукты в синтезе некоторых лекарственных средств.
Лит.: Клар Э., Полициклическне углеводороды, пер. с англ., т. 2, М., 1971, с. 292–301; Соколов В.3., Харлампович Г.Д., Производство и использование ароматических углеводородов, М., 1980; Ullmann's Encyklopadie; 4 Aufl., Bd 14, Weinheim, 1977, S. 685.
Н. Н. Артамонова
Значения в других словарях
- Флуорантен — См. Углеводороды ароматические. Энциклопедический словарь Брокгауза и Ефрона
