галоформная реакция
ГАЛОФОРМНАЯ РЕАКЦИЯ (галоформное расщепление)
расщепление соед., содержащих ацетильную группу, под действием щелочи и галогена (или гипогалогенита) на карбоновые кислоты, в молекулах которых на один атом С меньше, чем в исходном соед., и на галоформ (хлороформ, бромоформ или йодоформ), напр.:
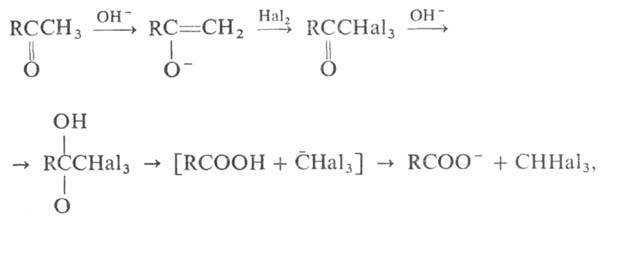
где R = H, Alk, алкенил; Hal = Cl, Br, I.
Реакцию проводят при 0–20 °C (реже при 50–70 °C) в воднодиоксановом растворе или в воде при строгом контроле pH. Выходы галоформа и карбоновой кислоты достигают 90%, но уменьшаются, если R в алкилметилкетоне содержит атомы Н, легко замещаемые на галоген, или если реакцию проводят в слишком разбавленных растворах. В последнем случае в качестве побочного продукта может образовываться тетрагалогенид углерода:
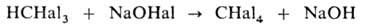
С трудом расщепляются кетоны, содержащие заместители, экранирующие карбонильную группу, напр. о, о-дизамещенные ацетофенона. В этом случае тригалогенопроизводные кетонов можно легко выделить, т. к. их расщепление достигается только при длительном кипячении с конц. растворами щелочей.
Реакция, подобная Г. р.,-разложение галогенкетонов действием фенолов в присутствии каталитич. количеств алкоголятов или RCOOK, напр.:
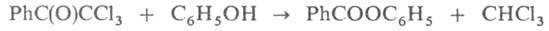
С галогенирующими агентами с образованием галоформов реагируют также этанол и некоторые др. спирты, которые в условиях Г. р. на промежут. стадии окисляются до ацетальдегида и алкилметилкетонов. По такому же механизму, как Г. р., реагируют α-и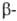 кетоэфиры и
кетоэфиры и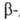 дикетоны. В этом случае галогенируются не метильные, а метиленовые или метиновые группы, напр.:
дикетоны. В этом случае галогенируются не метильные, а метиленовые или метиновые группы, напр.:
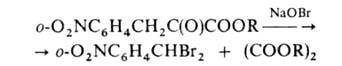
Г. р. используют для получения пивалиновой, трет-бутилуксусной и некоторых двухосновных (напр., алкилянтарных) и ненасыщ. кислот, расщепление гексахлорацетона — для трихлорацетилирования спиртов, фенолов и аминов, напр.:
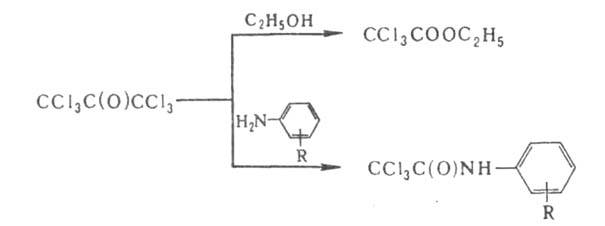
Иодоформная реакция применяется для доказательства структуры орг. соед. и количеств. анализа.
Лит.: Органикум, пер. с нем., [т.] 2, М., 1979, с. 35–37; Fuson R.C., Bull В.A., "Chem. Rev.", 1934, Bd 15, S. 275–309; Freedlander R.S. [a.o.j, "J. Organ. Chem.", 1981, v. 46, № 17, p. 3519–21.
Г. А. Артамкина
