галогенкарбоновые кислоты
ГАЛОГЕНКАРБОНОВЫЕ КИСЛОТЫ
содержат в молекуле карбоксильную группу и атомы галогенов. Назв. Г. к. производят от назв. карбоновых кислот с указанием числа атомов галогена и их положения относительно карбоксильной группы, напр. ClCH2COOH-хлоруксусная кислота, CH2ClCHClСООН -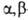 -дихлорпропионовая.
-дихлорпропионовая.
Г. к. вступают в реакции, характерные для карбоновых кислот и галогензамещенных углеводородов. Взаимное влияние атома галогена и группы COOH быстро уменьшается с удалением их друг от друга. Так, кислотность снижается в ряду α-Г. к., 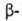 Г. к.,
Г. к., 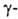 Г. к. Тригалогенуксусные кислоты легко декарбоксилируются. Карбоксильная группа сильно увеличивает способность галогена к нуклеоф. замещению: На1CH2COOH + НА → АCH2COOH + HHal, где А = OH, OR, NH2, SH, CN. Под действием водных растворов щелочей наряду с замещением атома галогена от
Г. к. Тригалогенуксусные кислоты легко декарбоксилируются. Карбоксильная группа сильно увеличивает способность галогена к нуклеоф. замещению: На1CH2COOH + НА → АCH2COOH + HHal, где А = OH, OR, NH2, SH, CN. Под действием водных растворов щелочей наряду с замещением атома галогена от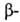 Г. к. отщепляется HHal, напр.: RCH(Hal)CH2COOH → RCH=CHCOOH + HHal. При гидролизе
Г. к. отщепляется HHal, напр.: RCH(Hal)CH2COOH → RCH=CHCOOH + HHal. При гидролизе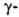 Г. к. и
Г. к. и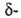 Г. к. образуются лактоны, напр.: ,
Г. к. образуются лактоны, напр.: ,
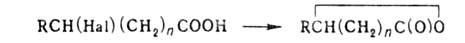
где n=2,3
Эфиры α-Г. к. при взаимодействии с карбонильными соед. в присутствии сильных оснований превращ. в эфиры глицидных кислот (реакция Дарзана), в присутствии Zn — в эфиры β-гидроксикарбоновых кислот (реакция Реформатского), напр.:
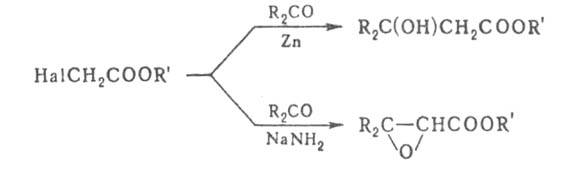
α- Г. к. и их производные присоединяются к непредельным соед. в присутствии трет-бутилпероксида: На1CH2COOH + RCH=CH2 → RCH2CH2CH(Hal)COOH, а также вступают с ними в реакцию теломеризации.
Методы получения Г. к.:
1. Введение галогена в карбоновые кислоты-прямое α-галогенирование кислот или их производных в присутствии катализаторов (реакция Гелля — Фольгарда — Зелинского); присоединение галогенов или галогеноводородов к непредельным кислотам; замещение гидроксигруппы гидроксикислот (оксикислот) галогеном и замещение галогена α-Г. к. другим галогеном. Перфторкарбоновые кислоты получают электрохим. фторированием.
2. Введение карбоксильной группы в галогенсодержащие соед. — окисление галогеноспиртов, галогенальдегидов, моно- и дигалогеналкенов; превращ. ди- и полигалогензамещенных (особенно содержащих разные галогены или одинаковые, но различающиеся подвижностью) в металлоорганические соединения с последующим их карбоксилированием; гидролиз дигалогенметиленовой и тригалогенметильной групп.
Многие Г. к. применяют в промышленности; так, монохлоруксусную кислоту — в производстве красителей, карбоксиметилцеллюлозы, 2,4-дихлор- и 2,4,5-трихлорфеноксиуксусных кислот. Дихлоруксусная и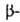 хлорпропионовая кислоты используются в синтезе лек. веществ (напр., пантотеновой кислоты),
хлорпропионовая кислоты используются в синтезе лек. веществ (напр., пантотеновой кислоты), 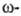 хлорэнантовая и
хлорэнантовая и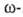 хлорпеларгоновая кислоты — для получения полиамидов, некоторые фторкислоты — для синтеза фторсодержащих полимеров. Na-Соли ряда Г. к. — гербициды. Na-Соль цис-3-хлоракриловой кислоты (акрофол) — дефолиант хлопчатника, Na-соль фторуксусной кислоты-инсектицид и родентицид.
хлорпеларгоновая кислоты — для получения полиамидов, некоторые фторкислоты — для синтеза фторсодержащих полимеров. Na-Соли ряда Г. к. — гербициды. Na-Соль цис-3-хлоракриловой кислоты (акрофол) — дефолиант хлопчатника, Na-соль фторуксусной кислоты-инсектицид и родентицид.
• см., напр. хлоруксусные кислоты, хлорпропионовые кислоты, фторуксусная кислота, трифторуксусная кислота, трифторнадуксусная кислота
Многие Г. к. обладают раздражающим действием; ПДК α- Г. к. 1–5 мг/м3, β-Г. к. 5–10 мг/м3. Эфиры низших Г.к.-ла-криматоры.
Лит.: Методы элементоорганичесхой химии. Хлор. Алифатические соединения, под общ. ред. А. Н. Несмеянова, К. А. Кочешкова, М., 1973; Общая органическая химия, пер. с англ., т. 4, М., 1983, с. 137–55.
Д. В. Иоффе
