Хэммонда постулат
ХЭММОНДА ПОСТУЛАТ
структура переходного состояния (ПС) в высокоэкзотермич. реакциях близка к структуре исходных реагентов (рис., кривая а), в сильно эндотермич. реакциях — к структуре продуктов (рис., кривая б). Используется для качеств. анализа положения ПС на координате реакции как одностадийных реакций, так и на каждой стадии многостадийных процессов. Х. п. часто применяют в более широком смысле — "расширенный постулат Хэммонда": с увеличением (уменьшением) экзотермичности реакции ПС сдвигается в сторону реагентов (продуктов).
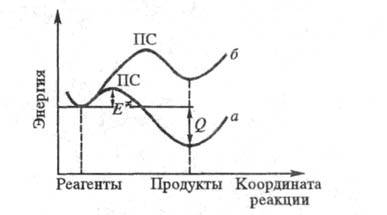
Положение переходного состояния для экзотермических (а) и эндотермических (б) реакций.
Для качеств. оценки положения ПС используют также т. наз. правило Торнтона, согласно которому при наличии факторов, способствующих стабилизации некоторой структуры, вклад ее в ПС становится больше. Так, в реакциях нуклеоф. замещения на атоме углерода в ПС может развиваться значительный положит. или отрицат. заряд. Изменение условий реакции, при которых стабилизируется, напр., положит. заряд, приводит к большему вкладу карбкатиона в структуру ПС.
Количеств. формулировкой Х. п. служит уравнение Маркуса, по которому энергия активации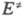 является квадратичной функцией теплового эффекта реакции Q (см. реакционная способность). При этом положение ПС, определяемое как
является квадратичной функцией теплового эффекта реакции Q (см. реакционная способность). При этом положение ПС, определяемое как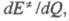 линейно зависит от экзотермичности реакции: с ее увеличением ПС сдвигается в сторону исходных реагентов.
линейно зависит от экзотермичности реакции: с ее увеличением ПС сдвигается в сторону исходных реагентов.
Сочетание Х. п. и правила Торнтона позволяет оценивать структуру и электронные характеристики ПС и прогнозировать влияние условий реакции и заместителей на скорость и направление процесса.
Предложен Дж. С. Хэммондом в 1955.
Лит.: Кери Ф., Сандберг Р., Углубленный курс органической химии, пер. с англ., кн. 1, М., 1981, с. 150–56; Марч Дж., Органическая химия, пер. с англ., М., 1987; Lowry T. H., Richardson К. S., Mechanism and theory in organic chemistry, 3 ed., N. Y., 1987.
И. В. Трушков
