иониты
ИОНИТЫ (ионообменники, ионообменные сорбенты)
полимерные вещества и материалы, содержащие ионогенные и (или) комплексообразующие группы, способные к обмену ионов при контакте с растворами электролитов. Большинство И. — твердые нерастворимые полиэлектролиты аморфной или кристаллич. структуры. Ионогенные группы закреплены на мол. каркасе (матрице) и диссоциируют, давая полиионы (фиксир. ионы) и подвижные противоионы, компенсирующие заряды полиионов. Например (для одной ионогенной группы):
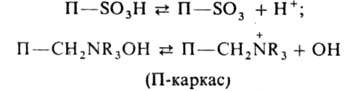
По знаку противоиона различают соотв. катиониты (поликислоты), аниониты (полиоснования) и полиамфолиты (амфотерные И., способные осуществлять как катионный, так и анионный обмен), по степени диссоциации ионогенных групп — слабо-, средне- и сильнокислотные (соотв. основные) катиониты (аниониты). При ионном обмене противоионы стехиометрически обмениваются на ионы электролита того же знака. Однако обменный процесс может сопровождаться побочными реакциями и адсорбцией молекул электролита (без расщепления на ионы). По хим. природе матрицы И. делят на орг., неорг. и минерально-орг., по происхождению — на природные и синтетические. Самый многочисл. класс — орг. И., из которых наиб. практич. применение получили синтетич. И. благодаря сочетанию высоких эксплуатационно-техн. характеристик с разнообразием способов получения и физ.-хим. свойств (см. ионообменные смолы). К орг. И. относятся также химически активированные угли, древесина, торф, целлюлоза. Неорг. И. имеют матрицу, состоящую из атомов элемента, связанных оксидными, фосфатными, цианидными фрагментами. Из неорг. И. наиб. значение имеют алюмосиликаты (пермутиты, мол. сита), в кристаллич. решетке которых имеются сравнительно большие пустоты. Чаще всего такие И. применяют для необратимого поглощения ионов; их недостаток — низкая устойчивость в кислой среде. Высокой селективностью обладают И, на основе гидратир. оксидов или гидроксидов некоторых элементов IV-VI гр. периодической системы, напр. SnO2.nH2O селективно сорбирует ионы Li+ и F−, Sb2O5.nH2O — ионы Na+. Фосфат Zr обладает свойством селективно сорбировать ионы Pb2+, Sr2+, Cs+, Ba2+; его применяют для удаления 90Sr и 137Cs из радиоактивных вод. Минерально-орг. И. состоят из орг. И. на минер. носителе или из неорг. И., диспергированного в полимерном связующем. Сочетают полезные свойства обоих видов И. Выпускают И. в виде гранул, порошков, волокон, нитей, нетканых ионообменных материалов, тканей, мембран ионообменных, растворов ионообменных полимеров (водорастворимые И.) и др. Характеризуют И. спец. параметрами, количественно описывающими способность к обмену и селективность при обмене в многокомпонентном растворе. Важнейшей количеств. характеристикой И. является обменная емкость — суммарное количество противоионов, приходящихся на единицу массы или объема И., в мг-экв/г(мл) или ммоль/г(мл). В зависимости от условий определения различают статич. и динамич. емкость. Коэф. распределения Р характеризует способность И. концентрировать извлекаемый компонент А; Р — отношение концентрации этого компонента в И. 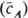 к его равновесному содержанию в растворе (cА):
к его равновесному содержанию в растворе (cА): 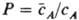 . Для характеристики сродства (избирательности) И. к определенному иону или компоненту раствора используют предельный коэф. распределения Р: при cА : 0.
. Для характеристики сродства (избирательности) И. к определенному иону или компоненту раствора используют предельный коэф. распределения Р: при cА : 0.
• см. также ионный обмен
Избирательность зависит от структуры И., хим. строения ионогенных групп и от того, в какой форме извлекаемый ион находится в растворе (напр., от степени его гидратации, размера, степени сольватации ионогенными и функц. группами). Макс. сольватация сорбируемого иона в фазе И. обеспечивает высокое сродство И. к этому иону. При сорбции крупных и сильно гидратир. ионов избирательность может определяться количеством и размером пор И., которые для синтетич. орг. И. зависят от типа и количества сшивающего агента и инертного растворителя, использованных при синтезе (см., напр., макропористые ионообменные смолы). Устойчивость И. к мех., термич. и радиац. воздействиям определяют как потерю основных физ.-хим. свойств (в % или долях) по отношению к исходным, осмотич. стабильность — по количеству (в %) нерастрескавшихся гранул И. после многократного воздействия на них циклов кислота — вода — щелочь (т. е. перехода из H+-формы в форму М+ ). Применяют И. для водоподготовки, выделения и концентрирования ценных и рассеянных элементов в гидрометаллургии, а также веществ из многокомпонентного орг. и биоорг. сырья, для очистки сточных вод и газовых выбросов от токсичных веществ, в производстве особо чистых веществ, для аналитич. и препаративных разделений биологически активных веществ, белков, вирусов, ДНК и РНК, в качестве носителей для гетерог. катализаторов хим. процессов. Тромборезистентные И. (гемосорбенты) используют для очистки крови, лимфы, ликвора от токсичных веществ.
Лит.: Гельферих Ф., Иониты, пер. с нем., М., 1962; Энциклопедия полимеров, М., т. 1–3, 1972–77; Иониты в цветной металлургии, М., 1975; Иониты в химической технологии, Л., 1982; Аширов А. А., Ионообменная очистка сточных вод, растворов и газов, Л., 1983. См. также лит. при ст. ионообменные смолы.
Ю. А. Лейкин
Значения в других словарях
- Иониты — Ионообменники, ионообменные сорбенты, твёрдые, практически нерастворимые вещества или материалы, способные к ионному обмену (См. Ионный обмен). Большая советская энциклопедия
- Иониты — (син. ионообменники) природные или синтетические твердые нерастворимые вещества, способные обменивать входящие в их состав ионы на ионы раствора, находящегося с ними в контакте; в медицине используются как лекарственные средства... Медицинская энциклопедия
- ИОНИТЫ — ИОНИТЫ (ионообменники) — твердые нерастворимые вещества, способные обменивать свои ионы с ионами внешней среды (ионный обмен). Подразделяются на аниониты и катиониты, обменивающие соответственно отрицательно или положительно заряженные ионы... Большой энциклопедический словарь
