изоцианаты
ИЗОЦИАНАТЫ
соед. общей формулы RN=C=O. Различают алкил-, арил-, гетерилизоцианаты (R — соотв. Alk, Ar, остаток гетероароматич. соед.), ацилизоцианаты RC(O)N=C=О, сульфонилизоцианаты RSO2N=C=O и элементоорг. И., содержащие атомы Si, Ge, So или Р, напр. (CH3)3SiN=C=0. Изоцианатная группа имеет строение, промежуточное между резонансными структурами 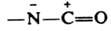
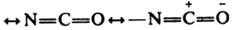 Она полярна, линейна, длина связи N=C 0,119, C=O 0,118 нм. В ИК спектре И. имеют характеристич. поглощение в области 2250–2270 см−1, в УФ спектре — при 220–250 нм. .
Она полярна, линейна, длина связи N=C 0,119, C=O 0,118 нм. В ИК спектре И. имеют характеристич. поглощение в области 2250–2270 см−1, в УФ спектре — при 220–250 нм. .
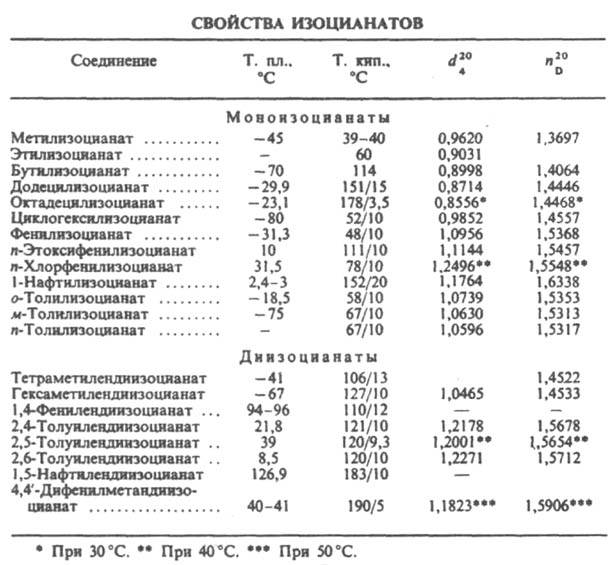
Многие И. — жидкости или твердые низкоплавкие вещества (см. табл.). И. высокотоксичны; многие — лакриматоры. Систематич. воздействие И. на организм повышает его чувствительность к ним. ПДК изоцианатов находится в пределах 0,05–1 мг/м3.
Химические свойства. И. — слабые основания, протонируются по атому кислорода. Наиб. характерно для них нуклеоф. присоединение. Нуклеоф. реагенты НА присоединяются по связи C=N:
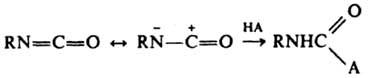
Ароматич. И. более реакционноспособны, чем алифатические. Электроноакцепторные заместители увеличивают реакц. способность, а электронодонорные понижают ее. opmo-Заместители в ароматич. ядре значительно понижают реакц. способность. Ацил- и сульфонилизоцианаты имеют повыш. реакц. способность. Со спиртами И. образуют уретаны:
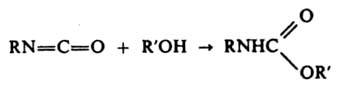
Эта реакция И. лежит в основе пром. синтеза полиуретанов из диизоцианатов и гликолей. Фенолы и тиолы реагируют так же, как спирты. И. легко реагируют с аминами, образуя замещенные мочевины:
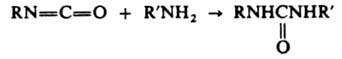
Аммиак, гидроксиламин, гидразин, амиды, уретаны, цианамид, мочевины, амидины, гуанидины, нитрамины, сульфонамиды реагируют аналогично. При взаимрд. И. с водой образуется соответствующая карбаминовая кислота, которая распадается с выделением CO2 и амина. Последний реагирует с И., образуя замещенные мочевины:
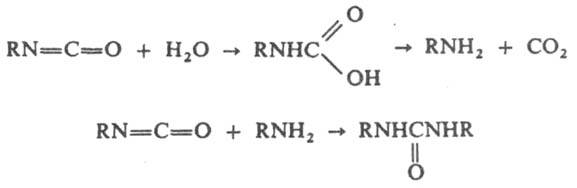
В щелочной среде реакция заканчивается на стадии образования амина, в кислой образуется аммониевая соль. Сероводород реагирует так же, как вода. На реакции И. с водой основано получение пенополиуретанов из низкомол. полиуретанов с концевыми изоцианатными группами или из смесей диизоцианатов и многоатомных спиртов. С карбоновыми кислотами И. образуют смешанные ангидриды, которые могут распадаться с образованием симметрич. ангидрида и амина:
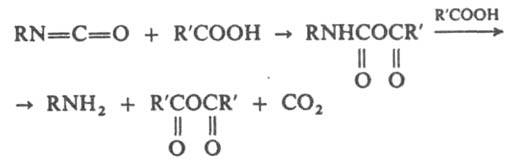
Продукты взаимод. И. с минеральными кислотами неустойчивы и при действии воды превращ. в аммониевые соли, напр.:
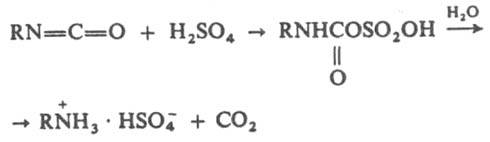
Ароматические И. при действии H2SO4 сульфируются в кольцо. При взаимодействии И. с пероксидами образуются азосоединения, напр.: RN=C=O + R'OOH → RNHC(O)OOR' → RN = NR + R'OH + CO2 Эта реакция используется для колориметрич. определения ароматич. И. и пероксидов. И. реагируют с соед., содержащими нуклеоф. центр на атоме С — цианид-ионом, металлоорг. соед., анионами CH-кислот, енаминами и др., напр.:
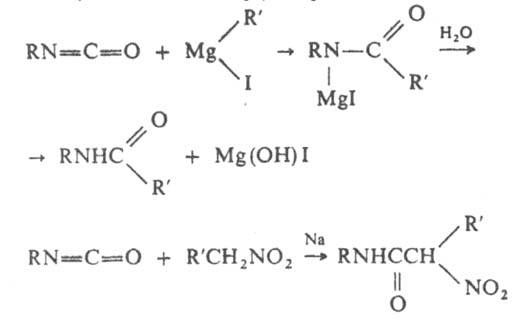
В реакции Фриделя — Крафтса И. образуют амиды, напр.:
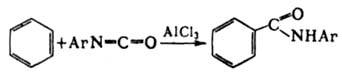
И. вступают в 1,2-циклоприсоединение со мн. соед., имеющими кратные связи, по схеме:
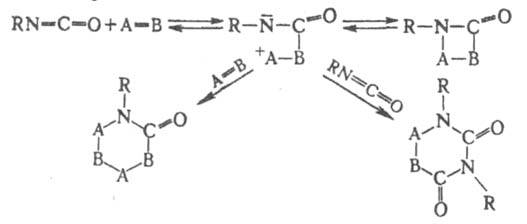
Так, напр., происходит димеризация и тримеризация И. Димеризация катализируется триалкилфосфинами, в меньшей степени третичными аминами. Димеры И. (1,2-азетидин-2,4-дионы) при повышенной температуре диссоциируют на мономеры:
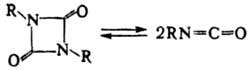
Тримеризация алифатич. и ароматич. И. ускоряется основаниями [CH3 COOK, (C2H5)3 N и др.]:
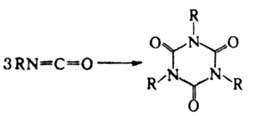
Тримеры И. (изоцианураты) устойчивы к нагреванию и имеют низкую реакц. способность. 1,2-Циклоприсоединение И. к кетонам, енаминам, не имеющим в β-положении атома Н, азометинам, виниловым эфирам приводит к различным гетероциклич. соед., напр.:
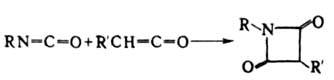
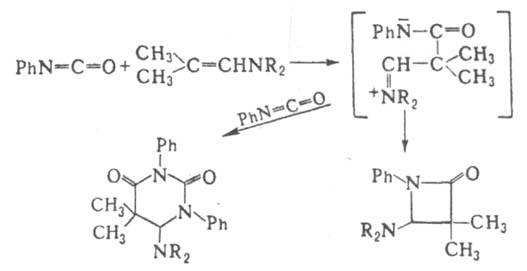
Многие др. соед. с кратными связями (альдегиды, тиокарбонильные соед., нитрозосоединения, алкилиденфосфораны, фосфинимины и др.) реагируют с И. по механизму 1,2-циклоприсоединения, с послед. расщеплением цикла, напр.:
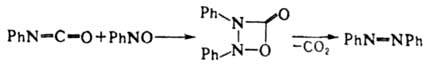
При нагр. в присутствии катализаторов [напр., R3PO, Fe(CO)5] И. превращ. по механизму 1,2-циклоприсоединения в карбодиимиды, напр.: 2ArN=C=O → ArN=С=NAr + CO2 Диизоцианаты образуют в этой реакции полимерные карбодиимиды. С эпоксидами, азиридинами и нитронами И. вступают в 1,3-циклоприсоединение, напр.:
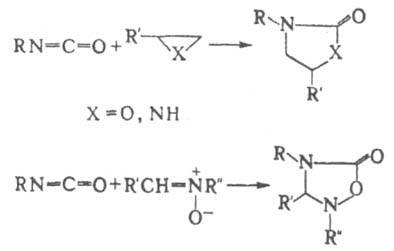
Ацилизоцианаты вступают в диеновый синтез, напр.:
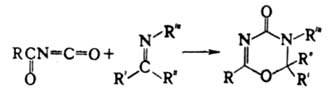
И. полимеризуются в органических растворителях с образованием [—NR—C(O)—]п. Процесс осуществляется при температурах от −20 до 100 °C; катализаторы — NaCN, NaNH2, (C2H5)3P, C2H5MgBr, C4H9Li. С этиленоксидом в присутствии (C2H5)3Al образуют полимер линейного строения:
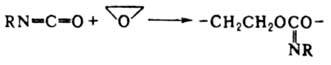
Для хим. анализа к И. добавляют вторичный амин (напр., дибутиламин) и определяют количество амина, не вступившего в реакцию.
Получение и применение. В промышленности И. получают фосгенированием аминов в высококипящем растворителе (напр., в о-дихлорбензоле) при избытке фосгена:
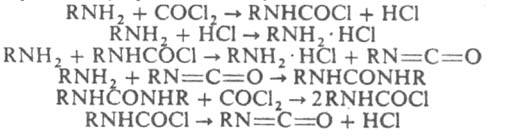
На первой стадии реакции при 0–60 °C образуются карбамоилхлорид и дизамещенная мочевина, которые при температуре 150–200 °C превращ. в И. Для предотвращения взаимод. образовавшегося И. с амином в некоторых случаях фосгенированию подвергают гидрохлорид или карбамат амина, напр.:
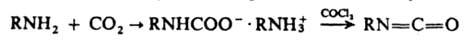
При фосгенировании силилзамещенных аминов И. образуются с высоким выходом в очень мягких условиях, напр.:
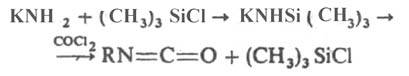
Перспективен метод синтеза И. действием CO на ароматич. нитросоединения в присутствии катализатора, напр. Co2(CO)8 или соед. Pd: PhNO2 + 3СО : PhN=C=O + 2CO2 И. могут быть получены термич. разложением уретанов или фосгенированием замещенных мочевин при нагр.:
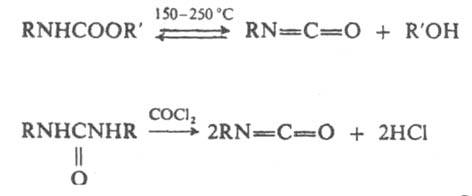
Для снижения температуры процесса и предотвращения обратной реакции используют силилзамещенные производные этих соед., напр.:
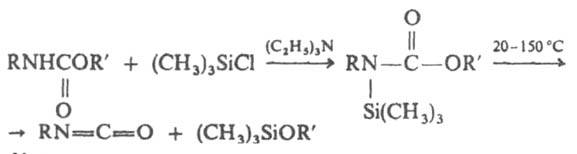
Уретаны и замещенные мочевины, так же как и некоторые др. продукты присоединения нуклеофилов к И., наз. изоцианатами блокированными (скрытыми). При нагр. до температуры разложения они выделяют свободный И. или реагируют подобно последнему. Важный препаративный метод получения И. — перегруппировка Курциуса (X = N3); перегруппировки Гофмана (X = NHHal) и Лоссена (X = NHOH) м. б. использованы при получении И., устойчивых в водной среде.
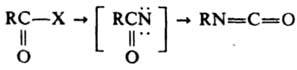
И. получают также по след. реакциям:
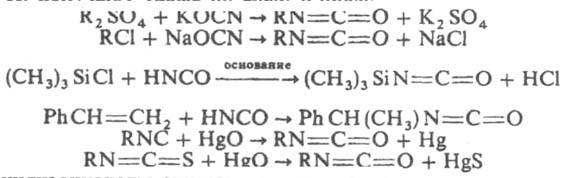
Ацилизоцианаты синтезируют по p-циям:
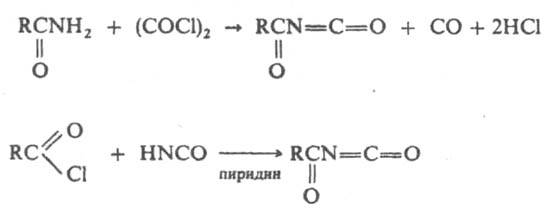
Сульфонилизоцианаты синтезируют аналогично, а также фосгенированием сульфамидов. И. используют для получения полиуретанов, в синтезе пестицидов — производных карбаминовой кислоты. Блокированные И. — компоненты пропиточных составов для текстильных материалов, вулканизующие агенты резиновых смесей, компоненты одноупаковочных полиуретановых лаков.
• см. также гексаметилендиизоцианат, метилизоцианат, толуилендиизоцианаты, 4,4'-дифенилметандиизоцианат
Лит.: Саундерс Дж. X., Фриш К. К., Химия полиуретанов, пер. с англ., ч. 1, М., 1968; Мономеры для поликонденсации, пер. с англ., М., 1976; Миронов В.Ф., Козюков В. П., "Ж. общ. хямии", 1984, т. 54, в.6, с. 1217–35; Обшая органическая химия, пер. с англ., т. 3. М., 1982, с. 629–46; Горбатенко В. И., Журавлев Е. 3., Самарай Л. И., Изоцианаты. Методы синтеза и физико-химические свойства алкил-, арил- и гетерилизоцианатов. К., 1987; Ozaki Sh., "Chem. Rev.", 1972, v. 72, № 5, p. 457–96.
Е. Ш. Каган
Значения в других словарях
- Изоцианаты — Эфиры изоциановой кислоты, R — N = С = О, где R — алифатический, ароматический, алкил-ароматический или гетероциклический радикал. И. — бесцветные или слабоокрашенные жидкости либо кристаллические вещества (см. таблицу). Большая советская энциклопедия
- ИЗОЦИАНАТЫ — ИЗОЦИАНАТЫ — RN-C-O, эфиры изоциановой кислоты (R — органический радикал); бесцветные жидкости, некоторые — кристаллические вещества. Получают реакцией первичных аминов RNH2 с фосгеном COCL2. Диизоцианаты OCN(R)nNCO применяют в производстве полиуретанов, лаков и клеев, гербицидов. Большой энциклопедический словарь
