изолобальной аналогии принцип
ИЗОЛОБАЛЬНОЙ АНАЛОГИИ ПРИНЦИП
служит для объяснения строения кластеров, сложных металлоорг. соед. и др. структур. И. а. п. заключается в том, что в реальных или воображаемых молекулах изолобальные группы взаимно заменяемы. Изолобальными наз. группы, имеющие одинаковое число граничных орбиталей (ГО высших занятых и низших вакантных мол. орбиталей) со сходными свойствами симметрии и пространств. строением, близкими значениями энергии и с одним и тем же числом электронов, занимающих эти ГО. Изолобальность групп А и Б изображается:
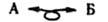
И. а. п. выявляет глубинное единство отдельных областей химии. В неявном виде И. а. п. применяется и в орг. химии, напр., изолобальны группы, имеющие одну работающую ГО с одним электроном
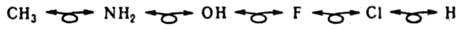
с двумя ГО и двумя электронами:
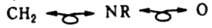
с тремя ГО и тремя электронами:

В химии металлоорг. соед. И. а. п. выполняет роль, аналогичную роли теории хим. строения в орг. химии. При таком использовании И. а. п. допустимо упрощение определения изолобальности: изолобальными можно назвать группы с одинаковым числом ГО и одинаковым числом электронов на них; при соблюдении этих условий примерное соответствие в пространств. строении, энергии и симметрии ГО обычно обеспечивается автоматически. При определении числа ГО металлоорг. фрагмента надо учитывать, что в отличие от элементов главных подгрупп переходные металлы имеют по девять валентных орбиталей. Отношения изолобальности между фрагментами металлоорг. соед. с соответствующим координац. числом металла n и орг. фрагментами приведены в таблице.

L — двухэлектронный лиганд, верх. индекс в металлоорг. фрагменте соответствует разности между числом валентных электронов металла и степенью его окисления. Для металлоорг соед. (октаэдрич. координация, n = 6) CH3-группе изолобальны группы d7ML5, напр. Mn(CO)5 или Fe(η5-C5H5)(CO)2 (т. к. C5H5 изолобальный аналог совокупности трех двухэлектронных лигандов); CH2-группе изолобальны группы d8ML4, напр. Ru(CO)4, СоСО(η5-C5H5), CH-группе группы d9ML3, напр. Со(CO)3, Ni(η5-C5H5). В соответствии с И. а. п. кластеры Re2(CO)10, Os3(CO)12, Ir4(CO)12 изолобальные аналоги этана, циклопропана и тетраэдрана соотв , а кластер [Fe2(CO)8]Sn изолобальный аналог спиропентана [т. к. Fe(CO)4 изолобален CH2 и Sn изолобален С]. И. а. п. может быть применена для предсказания возможности существования новых соединений. Достоверность таких прогнозов значительно повышается при использовании своеобразной "библиотеки" ГО металлоорг. фрагментов, изолобальных основным орг. фрагментам. Принцип сформулирован Р. Хофманом в 1976.
Лит.: Hoffmann R., "Angеw Chem.". 1982, v. 21, №10, p. 711–724; Stone F.G.A., "Angew Chem.", 1984, v. 23, № 2. p. 89-99
Н. П. Гамбарян, И. В. Станкевич
