электродные процессы
ЭЛЕКТРОДНЫЕ ПРОЦЕССЫ
физ.-хим. процессы, которые протекают на границе раздела проводников электрич. тока 1-го и 2-го рода и сопровождаются переходом через эту границу заряженных частиц — электронов и (или) ионов. При этом в качестве проводников 1-го рода могут выступать разл. металлы и сплавы, хим. соед., обладающие электронной проводимостью (напр., оксиды), а также полупроводниковые материалы; в качестве проводников 2-го рода выступают разл. ионные системы — растворы и расплавы электролитов, а также твердые электролиты.
Любой Э. п. всегда протекает в двух направлениях: в катодном, когда к границе раздела со стороны электрода течет отрицат. катодный ток (соответствующую плотность тока обозначают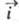 ), и в анодном, когда к границе раздела со стороны электрода течет положит. анодный ток (плотность тока
), и в анодном, когда к границе раздела со стороны электрода течет положит. анодный ток (плотность тока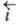 ). Суммарный Э. п. является катодным, если
). Суммарный Э. п. является катодным, если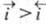 , и анодным, если
, и анодным, если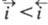 ; при этом измеряемая плотность тока
; при этом измеряемая плотность тока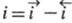 . Катодные процессы связаны с переносом электронов е от электрода к молекулам или ионам реагирующих на электроде веществ; последние при этом восстанавливаются. В анодных процессах, наоборот, происходит окисление реагирующих веществ, сопровождающееся переходом электронов на электрод либо растворением материала электрода. Хим. превращения в катодном процессе наз. электровосстановлением (напр., O2 + 4е + 4H+
. Катодные процессы связаны с переносом электронов е от электрода к молекулам или ионам реагирующих на электроде веществ; последние при этом восстанавливаются. В анодных процессах, наоборот, происходит окисление реагирующих веществ, сопровождающееся переходом электронов на электрод либо растворением материала электрода. Хим. превращения в катодном процессе наз. электровосстановлением (напр., O2 + 4е + 4H+ 2H2O), в анодном — электроокислением (напр., 2Cl− — 2е
2H2O), в анодном — электроокислением (напр., 2Cl− — 2е Cl2). В условиях электрохим. равновесия i =i и i = 0.
Cl2). В условиях электрохим. равновесия i =i и i = 0.
Обнаружить анодную составляющую катодного Э. п. можно с помощью радионуклидов. Так, если на амальгаме цинка, содержащей радионуклид Zn, в неактивном растворе ZnSO4 проводить катодный Э. п.
Zn2+ + 2e(Hg)  Zn(Hg), то через некоторое время раствор также
Zn(Hg), то через некоторое время раствор также
обнаруживает радиоактивность из-за наличия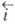 . Закон сохранения массы в ходе Э. п. отражают Фарадея законы.
. Закон сохранения массы в ходе Э. п. отражают Фарадея законы.
Важной особенностью Э. п. является их стадийный характер. Рассмотрим стадии Э. п. на примере реакции 2H3O+ + 2е(М)  H2 + 2H2O (М — металл). В стадии массопереноса ионы H3O+ из объема раствора переходят к поверхности металла М: (H3O+)об
H2 + 2H2O (М — металл). В стадии массопереноса ионы H3O+ из объема раствора переходят к поверхности металла М: (H3O+)об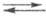 (H3O4)пов. Затем следует стадия вхождения ионов H3O+ в двойной электрический слой (их адсорбция на электроде): (H3O+)пов
(H3O4)пов. Затем следует стадия вхождения ионов H3O+ в двойной электрический слой (их адсорбция на электроде): (H3O+)пов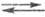 (H3O+)адс. После этого имеет место собственно электрохим. стадия разряда-ионизации: (H3O+)адс + е(М)
(H3O+)адс. После этого имеет место собственно электрохим. стадия разряда-ионизации: (H3O+)адс + е(М)  Hадс + H2O. Удаление адсорбированного водорода с поверхности электрода может осуществляться по трем параллельным путям:
Hадс + H2O. Удаление адсорбированного водорода с поверхности электрода может осуществляться по трем параллельным путям:
1) 2Hадс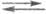 (H2)пов
(H2)пов
2) Hадс + е(М) + (H3O+)адс (H2)пов + (H2O)адс,
(H2)пов + (H2O)адс,
3) Hадс + е(М) + (H2O)адс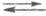 (H2)пов + (OH−)адс
(H2)пов + (OH−)адс
Путь (1) получил назв. рекомбинации, а пути (2) и (3) — электрохим. десорбции с участием соотв. ионов H3O+ и молекул воды. Затем следует стадия массопереноса растворенного H2 от поверхности металла в объем раствора: (H2)пов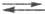 (H2)об. И, наконец, процесс завершается стадией образования новой фазы — пузырьков H2: (H2)об
(H2)об. И, наконец, процесс завершается стадией образования новой фазы — пузырьков H2: (H2)об (H2)газ. Если же в растворе имеется к.-л. орг. основание В (напр., пиридин), возникают дополнит. стадии: хим. взаимодействие — В + H3O+
(H2)газ. Если же в растворе имеется к.-л. орг. основание В (напр., пиридин), возникают дополнит. стадии: хим. взаимодействие — В + H3O+ ВH+ + H2O (в объеме раствора и на поверхности электрода), разряд адсорбированных частиц ВH+ и удаление продуктов с поверхности электрода.
ВH+ + H2O (в объеме раствора и на поверхности электрода), разряд адсорбированных частиц ВH+ и удаление продуктов с поверхности электрода.
Выяснение механизма Э. п. и определение скоростей как отдельных стадий, так и суммарного Э. п. составляет предмет электрохимической кинетики. Э. п. лежат в основе прикладной электрохимии.
Лит.: Дамаскин Б.Б., Петрий О. А., Введение в электрохимическую кинетику, 2 изд.. М., 1983.
Б. К. Дамаскин
Значения в других словарях
- Электродные процессы — Электрохимические превращения на границе электрод/электролит, при которых через эту границу происходит перенос заряда, проходит электрический ток. Большая советская энциклопедия
- ЭЛЕКТРОДНЫЕ ПРОЦЕССЫ — ЭЛЕКТРОДНЫЕ ПРОЦЕССЫ (электродные реакции) — связаны с переносом электронов через границу раздела фаз электрод — электролит. В зависимости от направления переноса электронов различают катодные и анодные электродные процессы... Большой энциклопедический словарь
