электролиз
ЭЛЕКТРОЛИЗ
совокупность электрохим. окислительно-восстановит. процессов, происходящих при прохождении электрич. тока через электролит с погруженными в него электродами. На катоде катионы восстанавливаются в ионы более низкой степени окисления или в атомы, напр.: Fe3+ + e Fe2+, Cu2+ + 2е
Fe2+, Cu2+ + 2е Cu (е — электрон). Нейтральные молекулы могут участвовать в превращениях на катоде непосредственно или реагировать с продуктами катодного процесса, которые рассматриваются в этом случае как промежут. вещества Э. На аноде происходит окисление ионов или молекул, поступающих из объема электролита или принадлежащих материалу анода; в последнем случае анод растворяется или окисляется (см. анодное растворение). Например:
Cu (е — электрон). Нейтральные молекулы могут участвовать в превращениях на катоде непосредственно или реагировать с продуктами катодного процесса, которые рассматриваются в этом случае как промежут. вещества Э. На аноде происходит окисление ионов или молекул, поступающих из объема электролита или принадлежащих материалу анода; в последнем случае анод растворяется или окисляется (см. анодное растворение). Например:
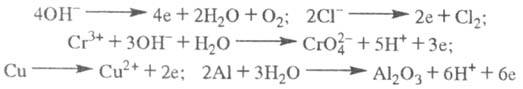
Э. включает два процесса: миграцию реагирующих частиц под действием электрич. поля к поверхности электрода и переход заряда с частицы на электрод или с электрода на частицу. Миграция ионов определяется их подвижностью и числами переноса (см. электропроводность электролитов). Процесс переноса неск. электрич. зарядов осуществляется, как правило, в виде последовательности одноэлектронных реакций, т. е. постадийно, с образованием промежут. частиц (ионов или радикалов), которые иногда существуют некоторое время на электроде в адсорбир. состоянии.
Скорости электродных реакций зависят от состава и концентрации электролита, материала электродов, электродного потенциала, температуры, гидродинамич. условий (см. электрохимическая кинетика). Мерой скорости служит плотность тока — количество переносимых электрич. зарядов через единицу площади поверхности электрода в единицу времени. Количество образующихся при Э. продуктов определяется Фарадея законами. Дня выделения 1 грамм-эквивалента вещества на электроде необходимо количество электричества, равное 26,8 А* ч. Если на каждом из электродов одновременно образуется неск. продуктов в результате ряда электрохим. реакций, доля тока (в %), идущая на образование продукта одной из реакций, наз. выходом данного продукта по току.
В электродном процессе участвуют вещества, требующие для переноса заряда наименьшего электрич. потенциала; это м. б. не те вещества, которые обусловливают перенос электричества в объеме раствора. Например, при Э. водного раствора NaCl в миграции участвуют ионы Na+ и Cl+, однако на твердых катодах ионы Na+ не разряжаются, а протекает энергетически более выгодный процесс разряда протонированных молекул воды: H3O+ + е — → 1/2H2 + H2O.
Применение Э. Получение целевых продуктов путем Э. позволяет сравнительно просто (регулируя силу тока) управлять скоростью и направленностью процесса, благодаря чему можно осуществлять процессы как в самых "мягких", так и в предельно "жестких" условиях окисления или восстановления, получая сильнейшие окислители и восстановители. Путем Э. производят H2 и O2 из воды, Cl2 из водных растворов NaCl, F2 из расплава KF в KH2F3.
Гидроэлектрометаллургия — важная отрасль металлургии цветных металлов (Cu, Bi, Sb, Sn, Pb, Ni, Co, Cd, Zn); она применяется также для получения благородных и рассеянных металлов, Mn, Cr. Э. используют непосредственно для катодного выделения металла после того, как он переведен из руды в раствор, а раствор подвергнут очистке. Такой процесс наз. электроэкстракцией. Э. применяют также для очистки металла — электролитич. рафинирования (электрорафинирование). Этот процесс состоит в анодном растворении загрязненного металла и в последующем его катодном осаждении. Рафинирование и электроэкстракцию проводят с жидкими электродами из ртути и амальгам (амальгамная металлургия) и с электродами из твердых металлов.
Э. расплавов электролитов — важный способ производства мн. металлов. Так, напр., алюминий-сырец получают Э. криолит-глиноземного расплава (Na3AlF6 + A12O3), очистку сырца осуществляют электролитич. рафинированием. При этом анодом служит расплав А1, содержащий до 35% Cu (для утяжеления) и потому находящийся на дне ванны электролизера. Средний жидкий слой ванны содержит BaCl2, A1F3 и NaF, a верхний — расплавленный рафинир. А1 и служит катодом.
Э. расплава хлорида магния или обезвоженного карналлита — наиболее распространенный способ получения Mg. В пром. масштабе Э. расплавов используют для получения щелочных и щел.-зем. металлов, Be, Ti, W, Mo, Zr, U и др.
К электролитич. способам получения металлов относят также восстановление ионов металла другим, более электро-отрицат. металлом. Выделение металлов восстановлением их водородом также часто включает стадии Э. — электрохим. ионизацию водорода и осаждение ионов металла за счет освобождающихся при этом электронов. Важную роль играют процессы совместного выделения или растворения неск. металлов, совместного выделения металлов и мол. водорода на катоде и адсорбции компонентов раствора на электродах. Э. используют для приготовления металлич. порошков с заданными свойствами.
Другие важнейшие применения Э. — гальванотехника, электросинтез, электрохимическая обработка металлов, защита от коррозии (см. электрохимическая защита).
Электролизеры. Конструкция пром. аппаратов для проведения электролитич. процессов определяется характером процесса. В гидрометаллургии и гальванотехнике используют преим. т. наз. ящичные электролизеры, представляющие собой открытую емкость с электролитом, в которой размещают чередующиеся катоды и аноды, соединенные соотв. с отрицат. и положит. полюсами источника постоянного тока. Для изготовления анодов применяют графит, углеграфитовые материалы, платину, оксиды железа, свинца, никеля, свинец и его сплавы; используют малоизнашивающиеся титановые аноды с активным покрытием из смеси оксидов рутения и титана (оксидные рутениево-титановые аноды, или ОРТА), а также из платины и ее сплавов. Для катодов в большинстве электролизеров применяют сталь, в т. ч. с разл. защитными покрытиями с учетом агрессивности электролита и продуктов Э., температуры и др. условий процесса. Некоторые электролизеры работают в условиях высоких давлений, напр., разложение воды ведется под давлением до 4 МПа; разрабатываются электролизеры и для более высоких давлений. В совр. электролизерах широко применяют пластич. массы, стекло и стеклопластики, керамику.
Во мн. электрохим. производствах требуется разделение катодного и анодного пространств, которое осуществляют с помощью диафрагм, проницаемых для ионов, но затрудняющих мех. смешение и диффузию. При этом достигается разделение жидких и газообразных продуктов, образующихся на электродах или в объеме раствора, предотвращается участие исходных, промежут. и конечных продуктов Э. в реакциях на электроде противоположного знака и в приэлектродном пространстве. В пористых диафрагмах через микропоры переносятся как катионы, так и анионы в количествах, соответствующих числам переноса. В ионообменных диафрагмах (мембранах) происходит перенос либо только катионов, либо анионов, в зависимости от природы входящих в их состав ионогенных групп. При синтезе сильных окислителей используют обычно без-диафрагменные электролизеры, но в раствор электролита добавляют K2Cr2O7. В процессе Э. на катоде образуется пористая хромит-хроматная пленка, выполняющая функции диафрагмы. При получении хлора используют катод в виде стальной сетки, на которую наносят слой асбеста, играющий роль диафрагмы. В процессе Э. рассол подают в анодную камеру, а из анодной камеры выводят раствор NaOH.
Электролизер, применяемый для получения магния, алюминия, щелочных и щел.-зем. металлов, представляет собой футерованную огнеупорным материалом ванну, на дне которой находится расплавленный металл, служащий катодом, аноды же в виде блоков располагают над слоем жидкого металла. В процессах мембранного получения хлора, в электросинтезе используют электролизеры фильтр-прессного типа, собранные из отд. рам, между которыми помещены ионообменные мембраны.
По характеру подключения к источнику питания различают монополярные и биполярные электролизеры (рис.). Монополярный электролизер состоит из одной электролитич. ячейки с электродами одной полярности, каждый из которых может состоять из неск. элементов, включенных параллельно в цепь тока. Биполярный электролизер имеет большое число ячеек (до 100–160), включенных последовательно в цепь тока, причем каждый электрод, за исключением двух крайних, работает одной стороной как катод, а другой как анод. Монополярные электролизеры обычно рассчитаны на большой ток и малые напряжения, биполярные — на сравнительно небольшой ток и высокие напряжения. Совр. электролизеры допускают высокую токовую нагрузку: монополярные до 400–500 кА, биполярные эквивалентную 1600 кА.
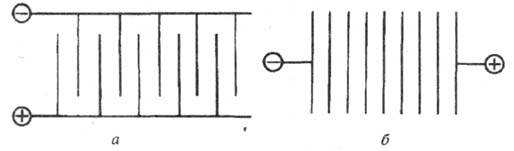
Схема подключения к источнику внеш. тока монополярного (а) и биполярного (б) электролизеров.
Лит.: Фиошин М.Я., Павлов В. Н., Электролиз в неорганической химии, М., 1976; Зимин В. М., Камарьян Г. М., Мазанко А.Ф., Хлорные электролизеры, М., 1984; Фиошин М.Я., Смирнова М. Г., Электрохимические системы в синтезе химических продуктов, М., 1985; Мазанко А.Ф., Камарьян Г.М., Помашин О.П., Промышленный мембранный электролиз, М., 1989; см. также лит. к ст. электросинтез, электрохимическая обработка металлов.
А. П. Томилов
Значения в других словарях
- электролиз — -а, м. Химические процессы, протекающие в электролитах и на погруженных в них электродах при прохождении через электролиты постоянного электрического тока. [От греч. ’ήλεκτρον — янтарь и λύσις — разложение] Малый академический словарь
- ЭЛЕКТРОЛИЗ — Совокупность электрохим. процессов, проходящих на электродах, погружённых в электролит, при прохождении по нему электрич. тока. В результате этих процессов в-ва, входящие в состав электролита, выделяются в свободном виде. Физический энциклопедический словарь
- Электролиз — (от Электро... и греч. lysis — разложение, растворение, распад) совокупность процессов электрохимического окисления-восстановления (См. Окисление-восстановление) на погруженных в электролит (См. Большая советская энциклопедия
- электролиз — орф. электролиз, -а Орфографический словарь Лопатина
- электролиз — Электр/о́/лиз/. Морфемно-орфографический словарь
- электролиз — ЭЛЕКТРОЛИЗ а, м. électrolyse f., > нем. Elektrolyse. Разложение веществ при помощи электрического тока на составные элементы (напр. воды на кислород и водород). Павленков 1911. Словарь галлицизмов русского языка
- ЭЛЕКТРОЛИЗ — ЭЛЕКТРОЛИЗ, ХИМИЧЕСКАЯ РЕАКЦИЯ, происходящая при прохождении постоянного тока через ЭЛЕКТРОЛИТ. Процесс заключается в перемещении положительных ионов к отрицательному ЭЛЕКТРОДУ (КАТОДУ) и отрицательных ионов к положительному электроду (АНОДУ). Научно-технический словарь
- электролиз — ЭЛЕКТРОЛИЗ -а; м. [от сл. электрический и lysis — разложение, отделение] Спец. Химические процессы (разложение, распад вещества), протекающие на погружённых в электролит электродах при прохождении электрического тока. ◁ Электролитический (см.). Толковый словарь Кузнецова
- электролиз — Электролиза, мн. нет, м. [от слова электрический и греч. lysis – растворение] (физ.). Разложение вещества на составные части при прохождении через его раствор электрического тока. Большой словарь иностранных слов
- ЭЛЕКТРОЛИЗ — ЭЛЕКТРОЛИЗ (от электро... и...лиз) — совокупность процессов электрохимического окисления — восстановления, происходящих на погруженных в электролит электродах при прохождении электрического тока. Большой энциклопедический словарь
- электролиз — электролиз м. Химический процесс разложения вещества на составные части при прохождении через него электрического тока. Толковый словарь Ефремовой
- электролиз — ЭЛЕКТР’ОЛИЗ, электролиза, мн. нет, ·муж. (от слова электрический и ·греч. lysis — растворение) (физ.). Разложение вещества на составные части при прохождении через его раствор электрического тока. Толковый словарь Ушакова
- электролиз — ЭЛЕКТРОЛИЗ, а, м. (спец.). Разложение (растворение, распад) вещества на составные части при прохождении через него электрического тока. | прил. электролизный, ая, ое и электролитический, ая, ое. Толковый словарь Ожегова
- Электролиз — См. Электролитическая диссоциация и Электрохимия. Энциклопедический словарь Брокгауза и Ефрона
