этаноламины
ЭТАНОЛАМИНЫ
Различают моноэтаноламин (2-аминоэтанол, этаноламин, коламин), диэтаноламин (иминодиэтанол) и триэтаноламин (нитрилотриэтанол). Бесцв. вязкие гигроскопичные жидкости со специфич. аминным запахом, неограниченно смешиваются с водой, хорошо раств. в этаноле, бензоле, хлороформе, плохо — в гептане (табл.). Обладают свойствами аминов и спиртов.
СВОЙСТВА ЭТАНОЛАМИНОВ
таблица в процессе добавления
* В воздухе рабочей зоны.
Э. — слабые основания; с минер. и сильными орг. кислотами дают соли. Соли Э. с жирными кислотами — некристаллич. вещества, похожие на воск, используются в промышленности как эмульгаторы (этаноламинные мыла). Реакция моноэтаноламинов с 48 %-ной HBr приводит к виниламинам:
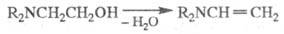
При взаимодействии со сложными эфирами и карбоновыми кислотами или их ангидридами и хлорат-нарядами моно- и диэтаноламины превращаются соотв. в N-(2-гидрооксиэтил)- и N,N-ди(2-гидрооксиэтил)амиды кислот. Триэтаноламин реагирует с карбоновыми кислотами и хлорангидридами при повышенных температурах, напр.:
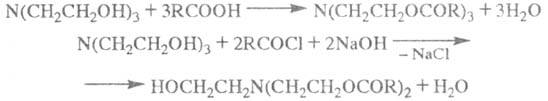
При реакции с дикарбоновыми кислотами моно- и диэтаноламины образуют полиэфирполиамиды [ —COCH(R)CONHCH2CH2O —]n, триэтаноламины — "сшитые" полиаминополиэфиры.
Моноэтаноламин с альдегидами (за исключением формальдегида) и кетонами дает шиффовы основания, последние обычно находятся в равновесии с изомерными оксазолидинами. Диэтаноламин с высшими альдегидами в присутствии K2CO3 образует третичные аминоспирты, которые далее превращаются в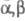 -ненасыщенные аминоспирты, напр.:
-ненасыщенные аминоспирты, напр.:
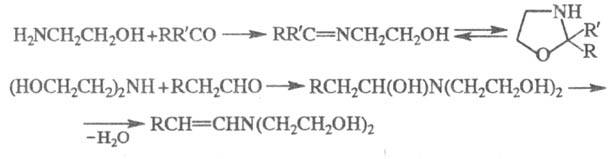
Реакция моно- и диэтаноламинов с формальдегидом в присутствии щелочи приводит к метилольным производным, последние могут вступать в реакцию со второй молекулой диэтаноламина с образованием N,N,N',N'-тетра(2-гидроксиэтил)метилендиамина, напр.:
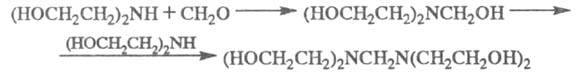
При взаимодействии солей моно- и диэтаноламинов с KCN или NaCN и альдегидами и кетонами образуются N-(гидроксиэтил)аминонитрилы, которые при гидролизе превращаются в N-(гидроксиэтил)аминокислоты, напр.:
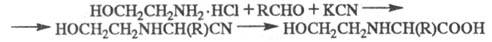
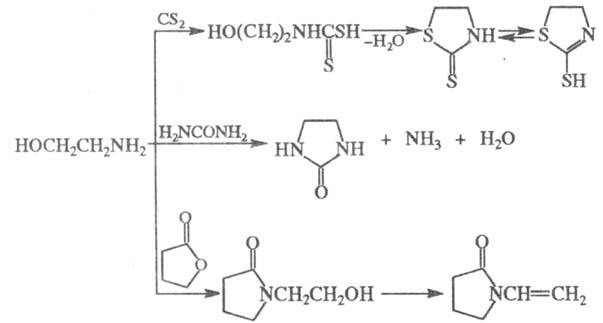
Моноэтаноламин при реакции с CS2 образует N-(2-гидроксиэтил)дитиокарбаминовую кислоту, которая при нагр. дает меркаптотиазолин; при нагр. с мочевиной — этиленмочевину; с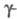 бутиролактоном — N-(2-гидроксиэтил)пирролидон, который далее превращается в N-винилпирролидон:
бутиролактоном — N-(2-гидроксиэтил)пирролидон, который далее превращается в N-винилпирролидон:
Моно- и диэтаноламины с безводным CO2 дают соответствующие N-гидроксиэтилкарбаминовые кислоты и их соли (напр., HOCH2CH2NHCOOH и HOCH2CH2NHCOOH x H2NCH2CH2OH), с акрилонитрилом — N-(2-гидроксиэтил)-аминопропионитрил (HOCH2CH2)2NCH2CH2CN, с этиленкарбонатом — уретановые гликоли HOCH2CH2OC(O)NH — -CH2CH2OH.
Аммонолиз моноэтаноламина в присутствии H2 и катализаторов гидрирования приводит к этилендиамину, диэтаноламин в тех же условиях превращается в пиперазин и полиэтиленполиамин:
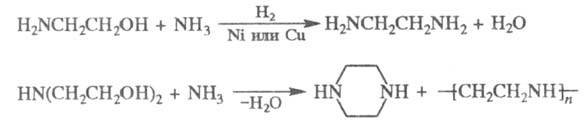
В промышленности Э. получают жидкофазным аммонолизом этиленоксида в присутствии небольшого количества воды. Процесс осуществляют в одну стадию (при температуре 90–130 °C и давлении 7–10 МПа). При соотношении этиленоксид : аммиак (1:15) продукт реакции содержит 78,3% моно-, 16% ди- и 4,4% триэтаноламинов. Конверсия этиленоксида 100%. Состав смеси Э. регулируют количеством NH3, температурой процесса и направлением в рецикл одного или двух Э. Образующуюся смесь Э., H2O и NH3 разделяют ректификацией, при этом аммиак в сжиженном виде направляется в рецикл; H2O, моно-, ди- и триэтаноламины выделяют ректификацией.
В лаборатории Э. синтезируют оксиэтилированием аммиака, аминированием этиленхлоргидрина, гидрированием метиленциангидрина.
Анализируют Э. методами ГЖХ, потенциометрич. титрования, колориметрии или иодометрии.
Э. применяют в качестве абсорбентов "кислых" газов (CO2, H2S, SO2 и др.) в процессах очистки технол. газов на предприятиях нефтеперерабатывающей, газодобывающей и хим. отраслей промышленности; как сырье для получения эмульгаторов, диспергаторов, стабилизаторов пен, моющих и чистящих средств, шампуней, ПАВ и др. Моноэтаноламин используют в орг. синтезе для получения этилендиамина, N-винилпирролидона и др., диэтаноламин — в производстве пластификаторов, ингибиторов коррозии и др.
Лит.: Справочник нефтехимика, т. 2, Л., 1978, с. 294; "Hydrocarb. processing", 1973, v. 52, № 11, p. 120; Kirk-Othmer encyclopedia, 3 ed., v. 1, N. Y., 1978, p. 944.
М. И. Якушкин
Значения в других словарях
- Этаноламины — Аминоспирты общей формулы RR'NCH2CH2OH. Известны моноэтаноламин, или коламин (R=R'=H), диэтаноламин (R=H, R'=CH2CH2OH) и триэтаноламин (R=R'=CH2CH2OH), имеющие tkип 171, 271 и 360°С и плотности при 20°С 1,0179, 1,0919 и 1,1258 г/см3 соответственно. Большая советская энциклопедия
- ЭТАНОЛАМИНЫ — ЭТАНОЛАМИНЫ — бесцветные вязкие жидкости: моноэтаноламин, или коламин, HOCH2CH2NH2 (tкип 171 °С) — диэтаноламин (HOCH2CH2)2NН (tкип 271 °С) — триэтаноламин (HOCH2CH2)3N (tкип 360 °С). Применяются, напр. Большой энциклопедический словарь
