кадмия галогениды
КАДМИЯ ГАЛОГЕНИДЫ
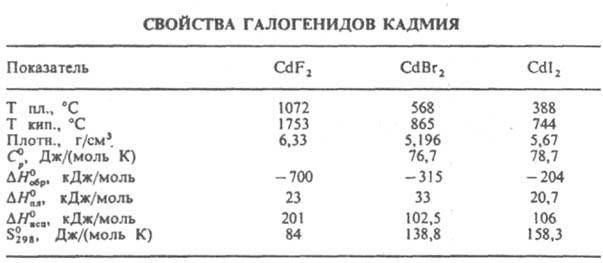
бесцветные кристаллы, расплав бромида желтый, иодида — коричневый. Свойства К. г. представлены в табл.
• см. также кадмия хлорид
Фторид CdF2 кристаллизуется в кубич. решетке типа флюорита (а = 0,541 нм, z = 4, пространственная группа Fm3m); уравнения температурной зависимости давления пара (в гПа): lgp = 10,397 — 14089/T(1092 — 1255 К); lgp = 27,62 — 16170/T + 5,03lg T(1345 — 2020 К). Раств. в воде (4,06% по массе при 20 °C, 1,80% при 100 °C). Не раств. в этаноле. Образует дигидрат CdF2.2H2O — кристаллы с ромбич. решеткой (а = 0,931 нм, b = 0,7078 нм, с = 0,8767 нм); устойчив на воздухе, разлагается выше 40 °C. Получают CdF2 действием HF на CdCO3. Оптич. материал, компонент стекол, люминофоров, лазерных материалов, твердых электролитов в хим. источниках тока. Бромид CdBr2 — чешуйчатые кристаллы с перламутровым блеском; существует в двух модификациях: ромбоэдрической (для гексагон. установки а = 0,3985 нм, с = 1,878 нм, z = 3, пространственная группа 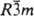 ) и гексагональной (а = 0,400 нм, с = 0,628 нм). Известно множество политипов. Очень гигроскопичен, хорошо раств. в воде (52,9% по массе при 25 °C, 61,4% при 100 °C). Ниже 36 °C из водных растворов кристаллизуется тетрагидрат (ΔH0обр −1494 кДж/моль), выше — безводный бромид. Хорошо раств. в метаноле (13,9% по массе при 20 °C) и этаноле (23,3% при 20 °C), плохо — в эфире, ацетоне. Получают CdBr2 бромированием Cd, действием HBr на CdCO3. Катализатор в орг. синтезе, стабилизатор фотоэмульсий, компонент вирирующих составов в фотографии.
) и гексагональной (а = 0,400 нм, с = 0,628 нм). Известно множество политипов. Очень гигроскопичен, хорошо раств. в воде (52,9% по массе при 25 °C, 61,4% при 100 °C). Ниже 36 °C из водных растворов кристаллизуется тетрагидрат (ΔH0обр −1494 кДж/моль), выше — безводный бромид. Хорошо раств. в метаноле (13,9% по массе при 20 °C) и этаноле (23,3% при 20 °C), плохо — в эфире, ацетоне. Получают CdBr2 бромированием Cd, действием HBr на CdCO3. Катализатор в орг. синтезе, стабилизатор фотоэмульсий, компонент вирирующих составов в фотографии.
Иодид CdI2 блестящие кристаллы в виде листочков с гексагон. слоистой решеткой (а = 0,4240 нм, с = 0,6855 нм, z = 1, пространственная группа 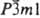 ). Известно также до 200 политипов, отличающихся последовательностью расположения слоев с гексагон. и кубич. плотнейшей упаковкой. Негигроскопичен. Хорошо раств. в воде (46,4% по массе при 25 °C, 56,1% при 100 °C). В интервале от −2,9 до −5,3 °C из водных растворов кристаллизуется тетрагидрат, который хорошо раств. в метаноле (67,4% по массе при 20 °C), этаноле (52,5% при 20 °C), ацетоне (29% при 20 °C), плохо в эфире и бензоле. Получают CdI2 иодированием Cd при нагр. или в присутствии воды, действием HI на CdCO3 или CdO. Катализатор в орг. синтезе, компонент пиротехн. составов, смазочных материалов. К. г. токсичны.
). Известно также до 200 политипов, отличающихся последовательностью расположения слоев с гексагон. и кубич. плотнейшей упаковкой. Негигроскопичен. Хорошо раств. в воде (46,4% по массе при 25 °C, 56,1% при 100 °C). В интервале от −2,9 до −5,3 °C из водных растворов кристаллизуется тетрагидрат, который хорошо раств. в метаноле (67,4% по массе при 20 °C), этаноле (52,5% при 20 °C), ацетоне (29% при 20 °C), плохо в эфире и бензоле. Получают CdI2 иодированием Cd при нагр. или в присутствии воды, действием HI на CdCO3 или CdO. Катализатор в орг. синтезе, компонент пиротехн. составов, смазочных материалов. К. г. токсичны.
Лит.: см. при ст. кадмий.
П. И. Федоров
