кальция бораты
КАЛЬЦИЯ БОРАТЫ
бесцветные кристаллы, плохо раств. в воде. Известно ок. 30 К. б.; свойства основных соед., образующихся в системе CaO — В2O3.H2O, приведены в таблице. Гексаоксодиборат трикальция Ca3(BO3)2 получают выше 165 °C гидротермальным способом, взаимод. оксидов Ca и В, пентаоксодиборат дикальция Ca2В2O5 гидротермальным способом при 285 °C. Дигидроксотетраоксодиборат дикальция Ca2[В2O4.(ОН)]ОН выделяют из растворов в щелочной среде; существует до 270 °C; из К. б. наименее раств. в воде (0,02% по массе в пересчете на В2O3); в природе — минерал сибирскит.
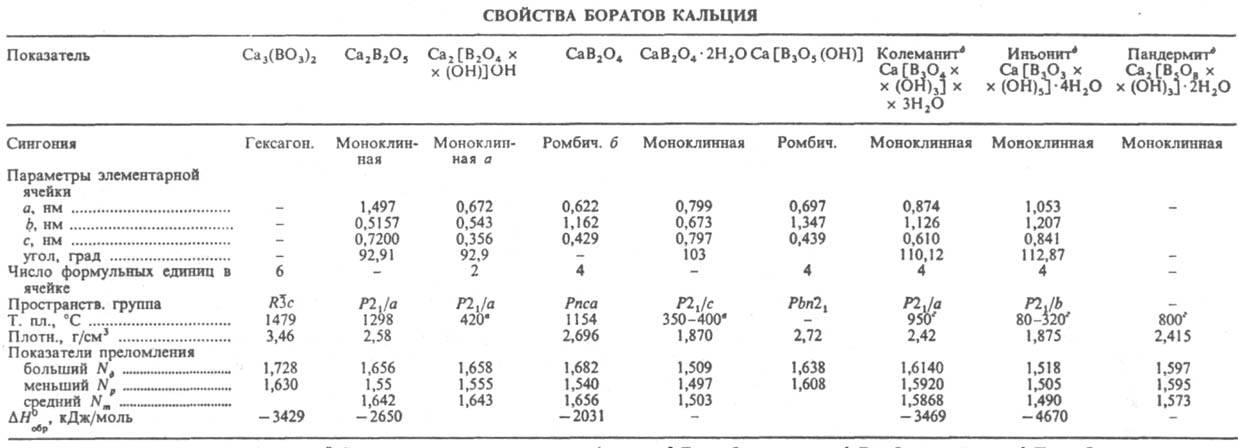
а Существует также др. модификация. б Существуют также еще три модификации. в Температура обезвоживания. г Для безводной соли. д Прир. бораты, остальные — синтетические.
Тетраоксодиборат (метаборат) кальция СаВ2O4 получают взаимод. Ca(OH)2 с H3BO3 в воде в виде ди-, тетра- и гексагидратов; в природе — минералы кальциборит (безводный), уралборит (дигидрат), фроловит (тетрагидрат), пентагидроборацит (пентагидрат) и др. Дигидрат тетраоксодибората кальция СаВ2O4.2H2O получают в промышленности осаждением Ca(OH)2 при pH 11,8 и 20 °C из растворов, образующихся после углекислотного разложения боросиликатного сырья. Гидроксопентаоксотриборат кальция Са[В3O5(ОН)] — аналог прир. минерала фабианита; пьезоэлектрик. Колеманит обезвоживается при 150–600 °C; твердость по Моосу 4,2. Твердость по Моосу иньонита 2, пандермита 3 (обезвоживается при 120–600 °C). Прир. К. б. встречаются в Турции, США, СССР. К. б. (природные и синтетические) применяют в производстве стекла, керамики, эмалей, как микроудобрения; прир. К.б. — сырье в производстве H3BO3.
Лит.: Годе Г. К., Бораты щелочноземельных металлов, Рига, 1986. См. также лит. при ст. бораты неорганические.
Г. Н. Кононова
