кальцийорганические соединения
КАЛЬЦИЙОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
содержат связь Са-С. Осн. типы — Са(R)Hal и CaR2. В твердом состоянии получены только некоторые Ca(R)Hal, их обычно используют в виде комплексов Ca(R)Hal.L, где L — ТГФ, эфир, (C2H5)3N и др. Соед. CaR2 — бесцв. или слегка окрашенные твердые вещества, устойчивые к нагреванию в вакууме; не раств. в углеводородах, раств. в эфире, ТГФ, диоксане [кроме Ca(CH3)2]. Соед. СаAr2 термически устойчивее, чем CaAlk2. Диметилкальций Ca(CH3)2 — вероятно, полимер, Са(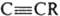 )2 димерны. В Ca(C5H5)2 связи Са—С имеют существенно ионный характер. По реакц. способности К. с. ближе к литийорг. соед., чем к магнийорганическим. Все К. с. и их растворы неустойчивы к действию кислорода и влаги [напр., Ca(CH3)2 быстро гидролизуется с разогреванием, Ca(C2H5)2 на воздухе тлеет]. К. с. металлируют орг. соед. с подвижным атомом водорода. Ca(Alk)Hal реагируют с CO2, давая Alk2CO и Alk3COH. Реакция Са(Ar)Hal с CO2 приводит к образованию ArСООН. К. с. с трудом присоединяются к изолированным кратным углерод-углеродным связям, легче — к сопряженным. К альдегидам и кетонам присоединяются с образованием соотв. вторичных и третичных спиртов. Ca(R)I с LiR' дают комплексы LiR'.Ca(R)I, которые более реакционноспособны, чем исходные К. с. CaR2 получают реакцией Ca с HgR2 в ТГФ или эфире, Са(CH=CH2)2 и Ca(CH2CH=CH2)2 — обменом между соответствующими R4Sn или R4Pb и Ca в присутствии следов HgBr2. Соед. Ca(R)Hal чаще всего синтезируют из Ca и RI в эфире или ТГФ в присутствии катализаторов; в ТГФ реакцию проводят при низких температурах во избежание побочной реакции Вюрца. К. с. получают также взаимод. CH-кислот с Ca или Ca(R)Hal, лучше в присутствии хелатирующих добавок. Ca(C5H5)2 м. б. получен соконденсацией паров Ca с C5H6 при −196 °C К. с. — компоненты катализаторов Циглера — Натты. Ca(C4H9)I и Ca(CPh3)Hal — инициаторы полимеризации. К. с. не нашли такого широкого применения в синтезе, как магний- и литийорг. соединения.
)2 димерны. В Ca(C5H5)2 связи Са—С имеют существенно ионный характер. По реакц. способности К. с. ближе к литийорг. соед., чем к магнийорганическим. Все К. с. и их растворы неустойчивы к действию кислорода и влаги [напр., Ca(CH3)2 быстро гидролизуется с разогреванием, Ca(C2H5)2 на воздухе тлеет]. К. с. металлируют орг. соед. с подвижным атомом водорода. Ca(Alk)Hal реагируют с CO2, давая Alk2CO и Alk3COH. Реакция Са(Ar)Hal с CO2 приводит к образованию ArСООН. К. с. с трудом присоединяются к изолированным кратным углерод-углеродным связям, легче — к сопряженным. К альдегидам и кетонам присоединяются с образованием соотв. вторичных и третичных спиртов. Ca(R)I с LiR' дают комплексы LiR'.Ca(R)I, которые более реакционноспособны, чем исходные К. с. CaR2 получают реакцией Ca с HgR2 в ТГФ или эфире, Са(CH=CH2)2 и Ca(CH2CH=CH2)2 — обменом между соответствующими R4Sn или R4Pb и Ca в присутствии следов HgBr2. Соед. Ca(R)Hal чаще всего синтезируют из Ca и RI в эфире или ТГФ в присутствии катализаторов; в ТГФ реакцию проводят при низких температурах во избежание побочной реакции Вюрца. К. с. получают также взаимод. CH-кислот с Ca или Ca(R)Hal, лучше в присутствии хелатирующих добавок. Ca(C5H5)2 м. б. получен соконденсацией паров Ca с C5H6 при −196 °C К. с. — компоненты катализаторов Циглера — Натты. Ca(C4H9)I и Ca(CPh3)Hal — инициаторы полимеризации. К. с. не нашли такого широкого применения в синтезе, как магний- и литийорг. соединения.
Лит.: Иоффе С. Т., Несмеянов А. Н., в кн.: Методы элементоорганической химии. Магний, бериллий, кальций, стронций, барий, под ред. А. Н. Несмеянова и К. А. Кочешкова, М., 1963; Landsell W. Е., в кн.. Comprehensive organometallic chemistry, v. 1, N. Y., 1982, p. 155–240.
А. С. Перегудов
