калия фосфаты
КАЛИЯ ФОСФАТЫ
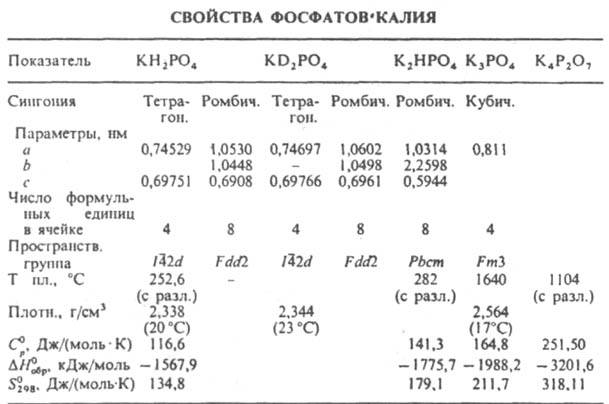
соли ортофосфорной кислоты — дигидрофосфат KH2PO4 и дидейтерофосфат KD2PO4, гидрофосфат K2HPO4, фосфат K3PO4; конденсир. фосфаты — циклофосфаты с циклич. анионом (КPO3)x, где х = 3, 4, 6, и линейные полифосфаты Kn + 2РnO3n + 1. Дигидрофосфат и дидейтерофосфат — бесцветные кристаллы (см. табл.); выше точки Кюри (для KH2PO4 −151,18 °C, для KD2PO4 −53,19 °C) устойчива тетрагон. модификация, ниже точки Кюри — ромбическая; сегнетоэлектрики. Для KH2PO4 макс. спонтанная поляризация 5,1 мкКл/см2; ε11 44 (в направлении оси x), ε33 20 (в направлении оси z), тангенс угла диэлектрич. потерь 10−3; оптически прозрачен в диапазоне 0,2–1,2 мкм; показатели преломления: больший Ng 1,5095, меньший Np 1,4684. Выше 250 °C плавится с разложением, образуя (КPO3)x. Раств. в воде (25,1 г в 100 г при 25 °C), практически не раств. в этаноле. Температура плавления эвтектики с водой (13,2% по массе KH2PO4) −2,62 °C. Получают взаимод. H3PO4 с водным раствором KOH или K2CO3, реакцией H3PO4 с KCl при 500–600 °C.
Для KD2PO4 макс. спонтанная поляризация 6,1 мкКл/см2; ε11 50, ε33 40; оптически прозрачен в диапазоне 0,2–1,6 мкм; Ng ~ 1,51, Np ~ 1,47; твердость по Моосу 2,5, хрупок. Монокристаллы KH2PO4 и KD2PO4 модуляторы и преобразователи частоты в лазерной технике; KH2PO4 также компонент удобрений, пекарских порошков, пищ. дрожжей, жидких моющих средств, эмульгатор пищ. продуктов и составов для очистки нефтепродуктов, умягчитель воды. Гидрофосфат бесцв. гигроскопичные кристаллы; выше 250 °C превращ. в полифосфаты. Хорошо раств. в воде и этаноле. Образует кристаллогидраты с 6 и 3 молекулами воды; гексагидрат переходит при 14,3 °C в тригидрат, который при 48,3 °C полностью обезвоживается. Температура плавления эвтектики гексагидрата (36,8% по массе K2HPO4) с водой — 13,5 °C. Получают взаимод. H3PO4 с водным раствором KOH или K2CO3. Используют K2HPO4 для приготовления буферных растворов, как питательную среду для выращивания плесневых грибов, продуцирующих пенициллины, компонент пищ. дрожжей, антифризов и лекарственных средств. Фосфат бесцв. гигроскопичные кристаллы. Раств. в воде (79,2 г в 100 г при 7,5 °C, 148,1 г при 45,1 °C). Из водных растворов кристаллизуются нона-, гепта-, три- и сесквигидраты, плавящиеся инконгруэнтно соотв. при —6,6, 47,5, 156,5 и 203 °C. При сплавлении с Li3PO4 образует Li3PO4.2K3PO4 (т пл. 833 °C, с разл.), а с Na3PO4 — непрерывный ряд твердых растворов, миним. т. пл. 1240 °C (65 мол. % K3PO4). Получают аналогично K2HPO4. Применяют как компонент электролитов при получении каучуков методом эмульсионной полимеризации. Трициклофосфат (КPO3)3 (плотн. 2,47 г/см3), диполифосфат K4P2O7 и триполифосфат K5Р3O10 (т. пл. 641,5 °C, с разл.) — бесцветные кристаллы; гигроскопичны; хорошо раств. в воде; образуют кристаллогидраты. Получают дегидратацией KH2PO4 (циклофосфаты) и K2HPO4 (полифосфаты) при температуре выше 300 °C. Конденсир. фосфаты К — компоненты жидких моющих средств, антиоксиданты и бактерициды при консервировании мясных продуктов, добавки к жидкостям для бурения, краскам, ингибиторы коррозии.
Лит.: Продан Е. А., Продан Д. И., Ермоленко Н. Ф., Триполифосфаты и их применение, Минск, 1969; Корбридж Д., Фосфор. Основы химии, биохимии, технологии, пер. с англ., М., 1982.
Н. С. Рукк
Значения в других словарях
- Калия фосфаты — Калиевые соли фосфорных кислот, например KPO3; см. Фосфаты калия. Большая советская энциклопедия
- КАЛИЯ ФОСФАТЫ — КАЛИЯ ФОСФАТЫ — K3PO4, калийные соли фосфорных кислот. Большой энциклопедический словарь
