карбкатионы
КАРБКАТИОНЫ (карбокатионы)
орг. катионы с четным числом электронов, строение которых м. б. представлено (по крайней мере, формально) структурой с электронодефицитным атомом углерода, имеющим вакантную орбиталь (С+). Реальный электронный дефицит этого атома (карбкатионного центра) м. б. очень мал из-за взаимод. с окружающими структурными фрагментами (делокализация заряда). К. подразделяют на: 1) классические ("карбениевые ионы") производные CH3+, которые характеризуются малой степенью взаимод. между карбкатионным центром и структурными фрагментами в β- или более удаленных положениях (напр., соед. формулы I), и 2) неклассические ("карбониевые ионы") — обычно производные CH5+ — со значит. степенью такого взаимод., напр. соед. II.
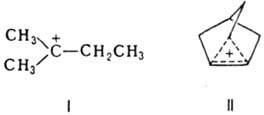
Термин "карбониевые ионы" ("ионы карбония") используют также для обозначения всех К. К. играют важную роль в орг. химии как интермедиаты мн. гетеролитич. реакций, имеющих теоретич. и прикладное значение (электроф. замещение в ароматич. ряду, электроф. присоединение, нуклеоф. замещение в алифатич. ряду, мол. перегруппировки, катионная полимеризация, каталитич. крекинг и др.). К. обычно образуются при действии электроф. реагентов, напр., протонных кислот, на орг. соединения (как правило, ненасыщенные; уравнения 1 и 2), при гетеролитич. разрыве связи (3), при разложении диазониевых катионов (4):
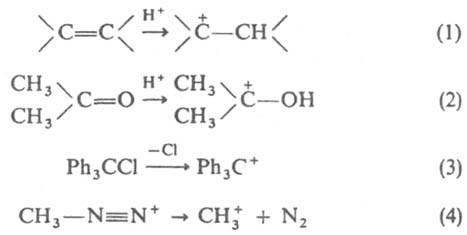
В газовой фазе К. образуются, напр., при ионизации электронным пучком в масс-спектрометре. Т. наз. долговечные К. генерируют обычно протонированием сравнительно слабоосновных орг. соед. в сверхкислых средах (HSO3F-SbF5, HF-SbF5 и др.) при низких температурах. Относит. устойчивость К. зависит от их строения и изменяется в очень широких пределах, увеличиваясь по мере увеличения степени делокализации заряда. Эффективно делокализуют заряд ненасыщ. фрагменты (двойная связь, ароматич. кольцо и т. п.), заместители с неподеленными парами электронов (OR, NR2 и др.) или содержащие атом переходного металла (ферроценил и др.). К. — реакционноспособные частицы, они взаимод. с нуклеофилами, присоединяя их (напр., уравнения 5 и 6) или отщепляя протон (электрофил) (7):
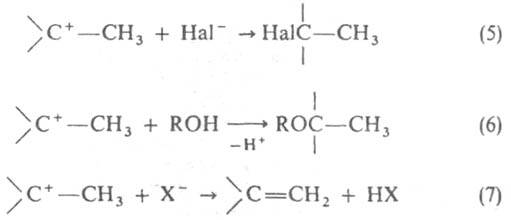
Многие К. склонны к перегруппировкам (взаимод. с "внутр. нуклеофилом"), протекающим обычно путем 1,2-сдвига к.-л. мигранта (разрешенная сигматропная реакция согласно правилам Вудворда — Хофмана):
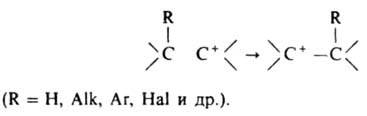
Разновидность К. — карбоксоний-катионы; в этих ионах карбкатионный центр обычно непосредственно связан с одной или неск. группами OR. Их строение м. б. описано двумя резонансными структурами:
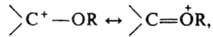
где R — H, Alk, Ar и др. или часть циклич. системы, как, напр., в пирилиевых катионах. К карбоксоний-катионам относятся и ацилий-катионы:
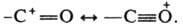
Лит.: Общая органическая химия, пер. с англ., т. 1, М., 1981, с. 511; Рахманкулов Д. Л., Ахматдинов Р. Т., Кантор Е. А., "Успехи химии", 1984, т. 53. в. 9. с. 1523–47; Carbonium ions, v. 1–5, N. Y., 1968- 76; Contemporary problems in carbonium ion chemistry, v. 1 2, В., 1984 (Topics in current chemistry, v. 116/117, 122).
В. Г. Шубин
Значения в других словарях
- КАРБКАТИОНЫ — КАРБКАТИОНЫ — ионы органических соединений, содержащие положительно заряженный атом углерода. Очень реакционноспособны и, как правило, неустойчивы в обычных условиях. Промежуточно образуются во многих химических реакциях, напр. при разложении некоторых диазосоединений. Большой энциклопедический словарь
