лактиды
ЛАКТИДЫ
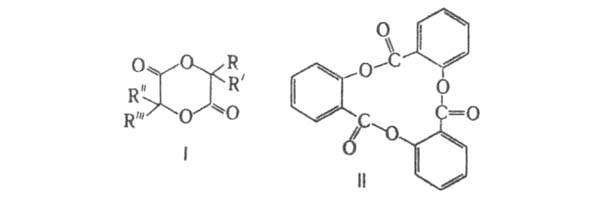
циклич. сложные эфиры α-гидроксикарбоновых кислот, содержащие две и более группировки —C(O)—О. Называют их как гетероциклич. соед. или в тривиальном назв. гидроксикислоты окончание преобразуют в окончание "ид". Умножающий префикс ("ди", "три" и т. д.) указывает на число молекул кислоты, образующих Л. Простейшие и наиб. изученные Л. — производные гликолевой кислоты (дигликолиды) общей формулы I (см. также табл.). Для этих соед. часто употребляют традиционные назв. без умножающих префиксов, напр. гликолид (в формулe I R-R'''=Н) и лактид (I; R=R''=CH3 и R'=R'''= Н). Известны также Л. ароматич. и алициклич. кислот, напр. трисалицилид (формула II) с т. пл. 199 °C. ИК спектры Л. имеют характеристич. полосы в области 1670–1720 см−1 (C=O).
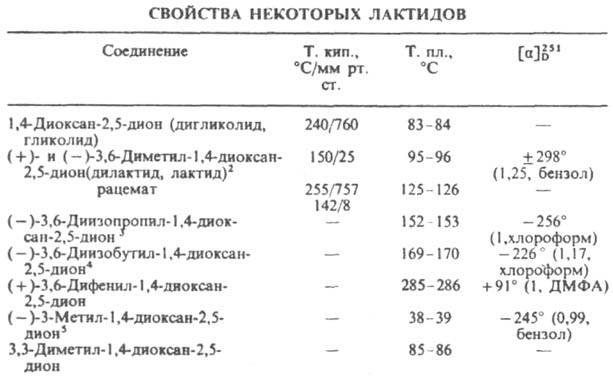
1 В скобках приведена концентрация в г/дл и указан растворитель. 2Т. пл. мезо-формы 42 °C. 3Т. пл. рацемата 134–135 °C. 4Т. пл. рацемата 138–140 °C. 5Т. пл. рацемата 64 °C. По химическим свойствам Л. подобны эфиром сложным. При взаимодействии с NH3 или аминами образуют амиды гидроксикислот, со спиртами — их эфиры; при кипячении с водой или щелочами легко гидролизуются в гидроксикислоты. Полимеризация дигликолидов приводит к образованию линейных полиэфиров общей формулы [—OC(RR')C(O)—]m. Осн. метод синтеза Л. — циклизация гидрокси- и галогенкарбоновых кислот или их щелочных солей в присутствии триэтиламина, ZnO, Zn-пыли, Sb2O3 или др. Реакцию проводят при высокой температуре в вакууме и получают циклич. олигоэфир, послед. деполимеризация которого приводит к смеси Л., разделяемой перегонкой в вакууме. Несимметричные Л. получают обычно дегидратацией смеси разл. гидроксикислот. Гликолид и лактид используют гл. обр. для получения полигликолида и полилактида, применяемых в медицине.
Лит.: Неницеску К. Д., Органическая химия, пер. с рум., т. 2, М., 1963, с. 109; Schulz R. С., Schwaab J., "Makromolec. Chem.", 1965. Bd 87, p. 90–102; Holten C. H., Lactic acid, N.Y., 1971, p. 221–24.
А. К. Хомяков
