ЛКАО-приближение
ЛКАО-ПРИБЛИЖЕНИЕ (приближение линейной комбинации атомных орбиталей)
широко используемое в квантово-хим. расчетах приближение, основанное на представлении мол. орбиталей (одноэлектронных волновых функций) ji линейными комбинациями атомных орбиталей ca: 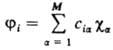 (α принимает значения от 1 до М, М — числоиспользуемых атомных орбиталей). Коэффициенты cia рассчитывают, напр., вариационным методом. Чем больше в этом представлении число независимых функций ca, тем лучше в общем случае аппроксимация мол. орбитали ji к точной волновой функции. Однако увеличение числа функций приводит к усложнению расчетов из-за быстрого возрастания числа молекулярных интегралов, которые используются в качестве отдельных слагаемых матричных элементов операторов физ. величин. ЛКАО-п. применяют в молекулярных орбиталей методах, конфигурационного взаимодействия методе и др. приближенных методах решения уравнения Шрёдингера для многоэлектронной мол. системы. Первоначально атомные орбитали в ЛКАО-п. являлись решениями задачи о движении электрона в поле одного центра (атомного ядра). Каждая атомная орбиталь ca обеспечивала правильное поведение волновой функции ji вблизи того ядра, которое является центром для этой атомной орбитали. К тому же атомные орбитали ca обеспечивали и асимптотически правильное поведение многоэлектронной волновой функции, составленной из мол. орбиталей ji, на больших расстояниях от ядра атома или системы ядер молекулы. Однако в ходе послед. развития расчетных методов квантовой химии функции ca постепенно утратили смысл волновых функций (орбиталей), получаемых при решении одноэлектронной атомной задачи, и стали играть роль лишь базисных функций, по которым проводится разложение мол. орбиталей, входящих в волновую функцию многоэлектронной системы. Базисные функции при этом специально подбирают таким образом, чтобы ЛКАО-п. наилучшим образом аппроксимировало поведение мол. орбиталей либо в областях между ядрами, либо во внешней по отношению к ядрам области, либо вблизи к.-н. определенного ядра и т. п. Таковы, напр., гауссовы базисные функции (см. орбиталь). Часто в состав линейных комбинаций включают не только орбитали ca, центрированные на ядрах, но и орбитали, центры которых не совпадают с положениями ядер. Например, м. б. использованы орбитали, которые находятся посредине между ядрами (т. наз. связевые орбитали), либо орбитали, имеющие единый центр для всей молекулы (одноцентровое приближение). Такое разнообразие базисных функций, как правило, встречается только в неэмпирических методах квантовой химии. В полуэмпирических методах и при интерпретации расчетных данных традиционные атомные орбитали в ЛКАО-п. продолжают сохранять свое значение, т. к. они позволяют достаточно просто оценить распределение электронной плотности около отдельных атомов и в областях между атомами (по хим. связям), а также изменение этого распределения при внеш. воздействиях на молекулу, в частности при элементарном акте хим. реакции (см. динамика элементарного акта). Простая интерпретация мол. структуры на базе ЛКАО-п. даже при использовании сложных многоконфигурационных электронных волновых функций позволяет отчетливее увидеть достоинства и недостатки этих функций.
(α принимает значения от 1 до М, М — числоиспользуемых атомных орбиталей). Коэффициенты cia рассчитывают, напр., вариационным методом. Чем больше в этом представлении число независимых функций ca, тем лучше в общем случае аппроксимация мол. орбитали ji к точной волновой функции. Однако увеличение числа функций приводит к усложнению расчетов из-за быстрого возрастания числа молекулярных интегралов, которые используются в качестве отдельных слагаемых матричных элементов операторов физ. величин. ЛКАО-п. применяют в молекулярных орбиталей методах, конфигурационного взаимодействия методе и др. приближенных методах решения уравнения Шрёдингера для многоэлектронной мол. системы. Первоначально атомные орбитали в ЛКАО-п. являлись решениями задачи о движении электрона в поле одного центра (атомного ядра). Каждая атомная орбиталь ca обеспечивала правильное поведение волновой функции ji вблизи того ядра, которое является центром для этой атомной орбитали. К тому же атомные орбитали ca обеспечивали и асимптотически правильное поведение многоэлектронной волновой функции, составленной из мол. орбиталей ji, на больших расстояниях от ядра атома или системы ядер молекулы. Однако в ходе послед. развития расчетных методов квантовой химии функции ca постепенно утратили смысл волновых функций (орбиталей), получаемых при решении одноэлектронной атомной задачи, и стали играть роль лишь базисных функций, по которым проводится разложение мол. орбиталей, входящих в волновую функцию многоэлектронной системы. Базисные функции при этом специально подбирают таким образом, чтобы ЛКАО-п. наилучшим образом аппроксимировало поведение мол. орбиталей либо в областях между ядрами, либо во внешней по отношению к ядрам области, либо вблизи к.-н. определенного ядра и т. п. Таковы, напр., гауссовы базисные функции (см. орбиталь). Часто в состав линейных комбинаций включают не только орбитали ca, центрированные на ядрах, но и орбитали, центры которых не совпадают с положениями ядер. Например, м. б. использованы орбитали, которые находятся посредине между ядрами (т. наз. связевые орбитали), либо орбитали, имеющие единый центр для всей молекулы (одноцентровое приближение). Такое разнообразие базисных функций, как правило, встречается только в неэмпирических методах квантовой химии. В полуэмпирических методах и при интерпретации расчетных данных традиционные атомные орбитали в ЛКАО-п. продолжают сохранять свое значение, т. к. они позволяют достаточно просто оценить распределение электронной плотности около отдельных атомов и в областях между атомами (по хим. связям), а также изменение этого распределения при внеш. воздействиях на молекулу, в частности при элементарном акте хим. реакции (см. динамика элементарного акта). Простая интерпретация мол. структуры на базе ЛКАО-п. даже при использовании сложных многоконфигурационных электронных волновых функций позволяет отчетливее увидеть достоинства и недостатки этих функций.
Лит. см. при статьях квантовая химия, орбиталь.
Н. Ф. Степанов
