малононитрил
МАЛОНОНИТРИЛ (динитрил малоновой кислоты, малонитрил, пропандинитрил, дицианометан) CH2(CN)2
мол. м. 66,07; бесцветные кристаллы; т. пл. 31,6–32,4 °C, т. кип. 218–219 °C;d435 1,0494; nD35 1,4130; μ 11,9∙10−30 Кл∙м; С°p 110 кДж/моль; ΔH0сгор −16,55 кДж/моль, ΔH0пл 10,06 кДж/моль, ΔH0обр −265,9 кДж/моль; S0298 131 Дж/(моль∙К); давление пара при 60 °C 200 Па; η 2,85 мПа • с (32,7 °C); γ 47,9 мН/м (37,5 °C); растворимость (г в 100 г): в воде 13,3, этаноле 40, диэтиловом эфире 20. М. обладает высокой реакц. способностью и широко применяется в орг. синтезе. Конденсация его с карбонильными соед. в условиях реакции Кнёвенагеля — общий метод получения дицианоолефинов:
CH2(CN)2 + RR'C = O → RR'C = C(CN)2
Эта реакция используется в синтезе 7,7,8,8-тетрацианохинодиметана и некоторых красителей. Соед. с дицианометиленовыми группами образуются также при реакциях М. с производными хинолиния, тропилия и циклопропенилия, напр.:
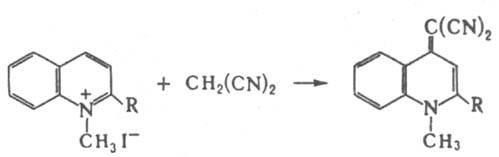
Бромирование М. приводит к диброммалононитрилу Br2С(СN)2 — промежут. продукту в синтезе тетрацианоэтилена, реакция с хлорцианом — к цианоформу HC(CN)3. При действии оснований М. димеризуется в 2-амино-1,1,3-трицианопропен, реакции которого приводят к производным разл. гетероциклич. соединений. В промышленности М. синтезируют взаимод. хлорциана с избытком ацетонитрила:
ClCN + CH3CN → CH2(CN)2 + HCl
Он м. б. также получен дегидратацией цианоацетамида действием P2O5 или POCl3. Качеств. анализ М. основан на образовании окрашенных соед. при реакции с фенантренхиноном или нитропрусеидом Na. Количеств. определение осуществляется с помощью ГЖХ или неводного потенциометрич. титрования. М. применяют в синтезе лекарственных средств, гербицидов, фунгицидов, дефолиантов, хлорбензальмалонодинитрила, красителей и пигментов и др. Его используют также как сшивающий агент для полимеров, добавку к смазочным маслам, стабилизирующую их вязкость, и комплексообразователь при извлечении золота. М. высокотоксичен; ЛД50 20–60 мг/кг (крысы, мыши, перорально). Т. всп. 112 °C.
Лит.: Freeman F., "Chem. Rev.", 1969, v. 69, № 5, p. 591–624; Fatiadi A. J, "Synthesis", 1978, № 3, p. 165–204; 1978, № 4, p. 241–82.
Д. В. Иоффе
