органосилазаны
ОРГАНОСИЛАЗАНЫ (силазаны)
кремнийорг. соединения со связями Si—N. Наиб. обширна группа моноциклических О. общей формулы (RR'SiNR'' (n = 2–4). Известны также полиэдрические О., напр. общей формулы [RSi(NR:)1,5]n (R, R', R: = алкил, арил, алкенил, п = 4 или 6).
О. — бесцв. или окрашенные жидкости, масла или кристаллич. вещества (см. табл.), некоторые из них — с резким раздражающим запахом. Олигомерные и полимерные О. — вещества от вазелиноподобных паст до твердых неплавящихся порошков. Большинство О. раств. в инертных органических растворителях. Для поли-О. с метильными, метилвинильными или метилфенильными группами у атомов Si характерны высокие термо- и влагостойкость, адгезия к стали от 20 до 75 кг/см2, tg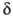 = 0,0006-0,0031,
= 0,0006-0,0031, 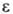 = 3,0–3,6 (20 °C, 106 Гц). Органоцик-лодисилазаны — одни из наиб. термостабильных кремнийорг. соединений. Линейные и циклические О. образуют комплексы с BF3, Al(C2H5)3, TiCl4; О., металлированные по атому N,-c диоксаном, диэтиловым эфиром, ТГФ, пиридином.
= 3,0–3,6 (20 °C, 106 Гц). Органоцик-лодисилазаны — одни из наиб. термостабильных кремнийорг. соединений. Линейные и циклические О. образуют комплексы с BF3, Al(C2H5)3, TiCl4; О., металлированные по атому N,-c диоксаном, диэтиловым эфиром, ТГФ, пиридином.
На воздухе О. гидролизуются. Стойкость О. к гидролизу обратно пропорциональна их основности; электроно-акцепторные заместители у атома азота снижают основность вплоть до полного исчезновения основных свойств, напр., у [(CH3)3Si]3N. При гидролизе О. с фрагментами
 образуются силоксановые связи (~ на 85%).
образуются силоксановые связи (~ на 85%).
В кислых средах скорость гидролиза увеличивается.
О. реагируют со спиртами, фенолами, кислотами и сила-нолами с расщеплением силазановой связи и образованием соответствующих алкокси-, арокси- и гидроксипроизводных и силоксановых группировок, напр.:
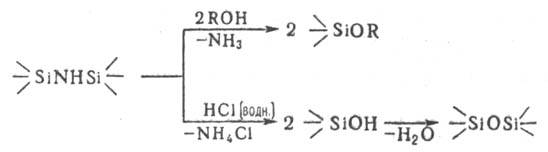
При действии HCl цикло-О. расщепляются до диоргано-дихлорсиланов и аммониевых солей. Переаминирование О. в зависимости от условий реакции приводит либо к диоргано-ди(органоамино)силанам, либо к новым N-замещенным циклич. соединениям:
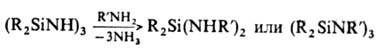
При действии изоцианатов (или изотиоцианатов) на О. образуются силилзамещенные мочевины.
Щелочные металлы (напр., в жидком NH3), их амиды, LiAlH4, орг. соед. Li и др. металлируют О. по атому N:
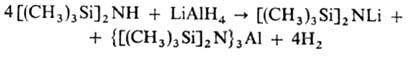
О., содержащие металлы подгруппы Zn, образуются реакцией обменного разложения в эфире:
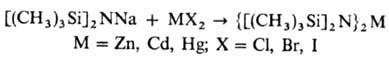
В промышленности линейные, циклич. и поли-О. получают аммо-нолизом или аминолизом моно-, ди- и трихлорорганосила-нов, напр.:
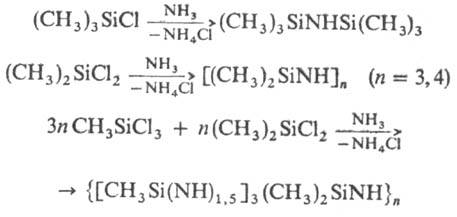
О. получают также гомоконденсацией аминосиланов:
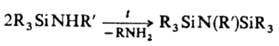
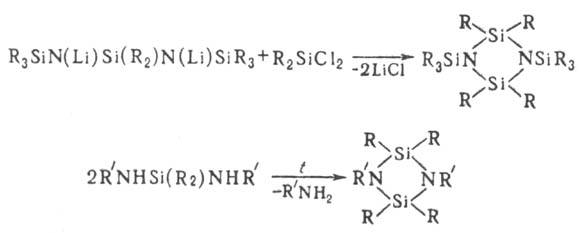
Для синтеза органоциклодисилазанов используют реакции обменного разложения, а для синтеза N-органилпроиз-водных О. — пиролиз диаминодиорганосиланов при 200–450 °C:
Поли-О. могут быть получены каталитич. поликонденсацией цикло-О. в присутствии гидроксидов металлов, NH4Br и др.
Применяют О. в производстве пластмасс (связующие и пропиточные составы), в качестве модификаторов резины для повышения диэлектрич. характеристик, адгезивов, отверди-телей эпоксидных смол, гидрофобизаторов кожи, шерсти, тканей, металлов; гексаметилдисилазан применяют для синтеза лек. препаратов, для модификации твердых носителей в ГЖХ, для т. наз. силильной защиты в орг. синтезе.
СВОЙСТВА НЕКОТОРЫХ ОРГАНОСИЛАЗАНОВ
таблица в процессе добавления
а Т.пл. 70–71 °C. б Т.пл. 183 °C. в 39 °C. г При 45СС.
Лит.: Борисов С. Н., Воронков М. Г., Лукевиц Э. Я., Кремнеэлементоорганические соединения. Л., 1966; Варежкин Ю. М., Синтез и применение полимеров циклодисилазановой структуры. Обзорная информация НИИТЭХИМ, М., 1977;Хананашвили Л. М., Андрианов К. А., Технология элементоорганических мономеров и полимеров, 2 изд., М., 1983.
В. Н. Емельянов
