перилен
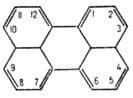
ПЕРИЛЕН
мол. м. 252,33; желтые кристаллы; т. пл. 277 279 °C, т. кип. 350 400 °C (с возг.); μ 1,5∙10−30 Кл∙м (бензол, 20 °C); хорошо раств. в ацетоне, CH3COOH, CHCl3, CS2, плохо в этаноле, бензоле, диэтиловом эфире; растворы обладают голубой флуоресценцией. Растворы в H2SO4 имеют зеленую окраску, переходящую на свету в результате фотоокисления в синюю, а затем красно-фиолетовую. Содержится в каменноугольной смоле и нефти.
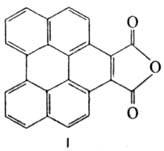
П. образует комплексы с пикриновой кислотой, нитробензолом, неорг. хлоридами, галогенами. Под действием HI и P восстанавливается в гексагидроперилен, под действием Na в амиловом спирте в октагидроперилен; при каталитич. гид-рировании над Pd превращ. в смесь гексагидро- и тетрагидропериленов. Реакции электроф. замещения протекают по положениям 3, 4, 9 и 10. Так, при действии H2O2 в HCl в нитробензоле П. образует смесь 3,9- и 3,10-дихлорпериленов; хлорирование в нитробензоле под действием AlCl3 приводит к тетрахлорперилену, обработка PCl5 к гексахлорперилену; бромирование Br2 в присутствии H2SO4 дает смесь 3,9- и 3,10-дибромпериленов. П. нитруется HNO3 в уксусном ангидриде до 3-нитроперилена, в CCl4 до 3,10-динитроперилена; сульфируется при нагр. с конц. H2SO4 в CH3COOH до смеси 3,9- и 3,10-периленсульфо-кислот; ацетилируется действием CH3COCl в присутствии AlCl3 до 3,9-диацетилперилена. Водной хромовой кислотой П. окисляется с образованием перилен-3,10-хинона; с малеиновым ангидридом образует ангидрид бензопериленкарбоновой кислоты (формула I).
Синтезируют П. нагреванием 2,2'-ди(1-гидрокси)нафтила при 400 500 °C в присутствии PCl5 и H3PO3 или 1,Г-ди-нафтила в присутствии AlCl3; конденсацией фенантрена с акролеином в присутствии HF с послед. дегидрированием и сплавле-нием с S; сплавлением нафталина с AlCl3.
Периленовое ядро лежит в основе некоторых особо прочных красителей, получаемых из антрахинона, напр. кубового темно-синего, кубового ярко-зеленого, однако сам П. в производстве красителей применения не находит.
Лит.: Клар Э.. Полициклические углеводороды, пер. с англ., т 2, M.. 1971, с. 61 73.
Н. Н. Артамонова
