S-аденозилметионин
S-АДЕНОЗИЛМЕТИОНИН [S-(5'-дезоксиаденозин-5'-ил)-метионин, активный метионин; активный метил]
донор метильных групп при трансметилировании (переносе метильных групп на разл. соединения-акцепторы), происходящем в клетках животных и растений. Мол. масса катиона А. 398,4; 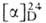 48,5° (1,8 г в 100 мл 5н. HCl);
48,5° (1,8 г в 100 мл 5н. HCl); 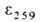 15,4∙103. Группа CH3 у атома S легко отщепляется; энтальпия реакции 41,868 кДж/моль.
15,4∙103. Группа CH3 у атома S легко отщепляется; энтальпия реакции 41,868 кДж/моль.
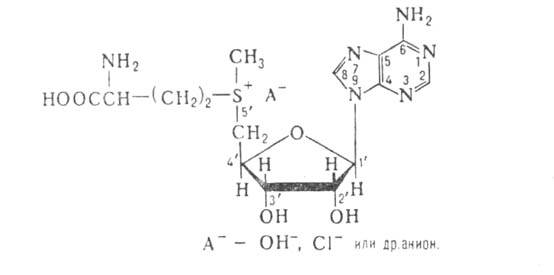
А. участвует в синтезе фосфатидилхолина, холина, адреналина, витамина В12 и др. Механизм трансметилирования-нуклеоф. замещение под действием ферментов группы метилтрансфераз, специфичных к акцепторам метильной группы. Метилируются обычно атомы N и О, реже — С.
Перенос метильных групп на двойные связи ненасыщ. жирных кислот микроорганизмов приводит к образованию кислот с разветвленной цепью или содержащих циклопропановые кольца. В результате метилирования некоторых биологически активных соед. (напр., гистамина, никотинамида) образуются продукты, выводимые из организма. В белках метилированию могут подвергаться аминогруппы остатков лизина и аргинина. Метилирование пуриновых и пиримидиновых оснований, а также рибозных колец — самая распространенная модификация нуклеиновых кислот, особенно транспортных РНК. В полисахаридах А. может, напр., метилировать атом О в положении 6 остатков D-глюкозы.
При элиминировании метильной группы А. превращается в S-аденозил-L-гомоцистеин, который гидролизуется до аденозина и гомоцистеина HSCH2CH2CH(NH2)COOH. Последний м. б. в организме метилирован при участии N5-метилтетрагидрофолиевой кислоты с образованием метионина, который вновь может включаться в состав А. Известны и другие пути метаболизма S-аденозил-L-гомоцистеина: у млекопитающих — расщепление с образованием гомосерина, аденина и 5-метилтиорибозо-1-фосфата, у микроорганизмов-дезаминирование аденозинового или гомоцистеинового фрагментов молекулы, а также отщепление аденина.
А. служит также донором аминопропильных фрагментов при биосинтезе аминов-спермина H2N (CH,)3NH (CH2)4NH (CH2)3NH, и спермидина H2N(CH2)3NH(CH2)4NH2, а также донором аминогруппы при синтезе биотина. Установлена регуляторная функция А. для некоторых ферментов: воздействие А. на одну из субъединиц фермента (напр., в результате переноса аденозильного остатка) меняет сродство к субстрату у другой.
Синтез А. в организме осуществляется замещением фосфорной компоненты АТФ L-метионином с отщеплением пирофосфорной и ортофосфорной кислот. Реакция катализируется метионин-аденозилтрансферазой. Таким же образом осуществляют препаративный синтез А.
Лит.: Lorn bardini J. В., Talalay P., "Advances in Enzyme Regulation", 1971, v. 9, p. 349–84; Cantoni G.L., "Annual Review of Biochemistry", 1975, v. 44, p. 435–51; UsdinE., Biochemistry of S-adenosylomethionine and related compounds, L, 1982.
Н. В. Гуляева
Значения в других словарях
- S-аденозилметионин — Производное метионина, представляющее его активную в метаболическом отношении форму; является донором лабильных метильных групп, дефицит которых в организме ведет к нарушению обмена веществ (жировому перерождению печени). Медицинская энциклопедия
