самарий
САМАРИЙ (обнаружен в минерале самарските, названном в честь рус. геолога В. Е. Самарского-Быховца; лат. Samarium) Sm
хим. элемент III гр. периодической системы; относится к редкоземельным элементам (цериевая подгруппа лантаноидов); ат. н. 62, ат. м. 150,36. Природный С. состоит из стабильных изотопов 144Sm (3,09%), 148Sm (11,27%), 149Sm (13,82%), 150Sm (7,47%). 152Sm (26,63%), 154Sm (22,53%) и радиоактивного изотопа l47Sm (15,07%, T1/2 1,3∙1011 лет, α-излучатель). Поперечное сечение захвата тепловых нейтрр-нов для прир. смеси изотопов 5,6∙10−25 м2. Конфигурация внеш. электронных оболочек атома 4f6 5s2 5p6 6s2; степени окисления + 3, +2 и, вероятно, +4; энергии ионизации при последоват. переходе от Sm0 к Sm5+ соотв. 5,63, 11,07, 23,43, 41,37, 62,7 эВ; электроотрицательность по Полингу 1,0–1,2; атомный радиус 0,181 нм, ионные радиусы (в скобках даны координац. числа) Sm2+ 0,136 нм (7), 0,141 нм (8), 0,146 нм (9), Sm3+ 0,110 нм (6), 0,116 нм (7), 0,122 нм (8), 0,127 нм (9), 0,138 нм (12).
Содержание в земной коре 7∙10−4% по массе, в морской воде 2,3∙10−6 мг/л. Вместе с др. РЗЭ содержится в минералах монаците, бастнезите (0,7–1,3% в пересчете на Sm2O3), лопарите, самарските, гадолините, ортите и некоторых др.
Свойства. С. — серебристо-желтый металл; α-Sm имеет три-гон. кристаллич. решетку, а = 0,8996 нм, α = 23,21°, z = 3, пространственная группа 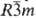 ; β-Sm кристаллизуется в кубич. решетке тина α-Fe, а = 0,407 нм, z = 2, пространственная группа Iт3т; температура перехода α
; β-Sm кристаллизуется в кубич. решетке тина α-Fe, а = 0,407 нм, z = 2, пространственная группа Iт3т; температура перехода α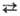 β 917 °C, ΔH перехода 3,1 кДж/моль; т. пл. 1072 °C, т. кип. 1788 °C; плотн. α-Sm 7,536 г/см3, плотн. β-Sm 7,40 г/см3;
β 917 °C, ΔH перехода 3,1 кДж/моль; т. пл. 1072 °C, т. кип. 1788 °C; плотн. α-Sm 7,536 г/см3, плотн. β-Sm 7,40 г/см3; 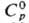 29,5 Дж/(моль∙К);
29,5 Дж/(моль∙К); 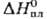 191,2 кДж/моль.
191,2 кДж/моль. 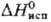 166,6 кДж/моль;
166,6 кДж/моль; 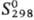 69,5 Дж/(моль∙К); давление пара 4,18 Па (1072 °C); ρ 5,2∙10−7 Ом∙м (73 К); точка Нееля 14 К; твердость по Бринеллю 450–600 МПа. Легко поддается механической обработке.
69,5 Дж/(моль∙К); давление пара 4,18 Па (1072 °C); ρ 5,2∙10−7 Ом∙м (73 К); точка Нееля 14 К; твердость по Бринеллю 450–600 МПа. Легко поддается механической обработке.
На воздухе С. окисляется медленно, при нагр. во влажном воздухе быстрее. С минеральными кислотами бурно реагирует, кипящей водой окисляется, взаимод. с галогенами, халькогенами, N2, H2 при нагревании. В водных средах существует в виде производных Sm(III); в присутствии сильных восстановителей способен переходить в Sm(II). В неводных средах и в твердых дигалогенидах Sm2+ относительно устойчив. Дигалогениды С. образуются при действии H2 или металлич. Sm на SmF3 или SmCl3; Sm2+ существует также в расплавах галогенидных смесей, содержащих металлический С.
Сесквиоксид Sm2O3-желтые кристаллы с кубич. решеткой типа Tl2O3 (а = 1,0932 нм, z = 16, пространственная группа Ia3); известна моноклинная модификация B-Sm2O3 (а = 1,4177 нм, b = 0,3633 нм, с = 0,8847 нм, β = 99,96 °, z = 6, пространственная группа С2/m), существующая выше 875 °C; т. пл. 2270 °C; 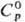 114,5 Дж/(моль∙К);
114,5 Дж/(моль∙К); 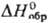 −1822,6 кДж/моль,
−1822,6 кДж/моль, 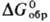 −1734,4 кДж/моль;
−1734,4 кДж/моль; 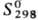 151 Дж/(моль∙К); получают разложением нитратов, сульфатов, оксалатов или др. кислородсодержащих соед. Sm на воздухе при 800–1000 °C; входит в состав разл. оксидных материалов, в т. ч. стекол, керамик, люминофоров и др. Временно допустимая концентрация в воздухе рабочей зоны 6,0 мг/м3 (класс опасности 3).
151 Дж/(моль∙К); получают разложением нитратов, сульфатов, оксалатов или др. кислородсодержащих соед. Sm на воздухе при 800–1000 °C; входит в состав разл. оксидных материалов, в т. ч. стекол, керамик, люминофоров и др. Временно допустимая концентрация в воздухе рабочей зоны 6,0 мг/м3 (класс опасности 3).
Трифторид SmF3-светло-желтые кристаллы. Существует в двух кристаллич. модификациях: с тритон. решеткой типа α-LaF3 (а = 0,6962 нм, с = 0,7128 нм, z = 6, пространственная группа Р3Сl, плотн. 6,90 г/см3) и с ромбической типа Fe3C (а = 0,6669 нм, b = 0,7059 нм, с = 0,4405 нм, z = 4, пространственная группа Рпта, плотн. 6,64 г/см3); температура полиморфного перехода 490 °C; т. пл. 1305 °C; 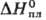 52,5 кДж/моль,
52,5 кДж/моль, 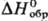 −1668,9 кДж/моль; получают осаждением из растворов солей Sm(III) фтористоводородной кислотой, фторированием Sm2O3 при нагр. и др. способами; применяют при получении чистого С. металлотермич. способом, как микродобавку при производстве фторидных стекол.
−1668,9 кДж/моль; получают осаждением из растворов солей Sm(III) фтористоводородной кислотой, фторированием Sm2O3 при нагр. и др. способами; применяют при получении чистого С. металлотермич. способом, как микродобавку при производстве фторидных стекол.
Три хлорид SmCl3-бледно-желтые кристаллы с гекса-гон. решеткой типа UC13 (а = 0,7378 нм, с = 0,4171 нм, z = 2, пространственная группа P63/m); т. пл. 678 °C; 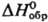 −1028 кДж/моль,
−1028 кДж/моль, 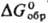 −942 кДж/моль;
−942 кДж/моль; 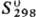 113 Дж/(моль∙К); образует кристаллогидраты; получают взаимод. смеси Cl2 и CCl4 с Sm2O3 или оксалатом С. выше 200 °C, обработкой SmCl3∙nH2O тионилхлоридом при кипячении с послед. возгонкой; безводный хлорид применяют для металлотермич. получения С., гидраты-для получения др. соединений С.
113 Дж/(моль∙К); образует кристаллогидраты; получают взаимод. смеси Cl2 и CCl4 с Sm2O3 или оксалатом С. выше 200 °C, обработкой SmCl3∙nH2O тионилхлоридом при кипячении с послед. возгонкой; безводный хлорид применяют для металлотермич. получения С., гидраты-для получения др. соединений С.
Получение. Концентрат, содержащий Sm, Eu, Gd, Tb и некоторые др. РЗЭ, разделяют зкстракцией, ионообменной сорбцией или же комбинир. методом (вместе с селективным восстановлением Eu). С. из полученных таким образом растворов осаждают в виде карбоната или оксалата и затем прокаливают до Sm2O3.
Осн. метод получения металлического С. — металлотермич. восстановление Sm2O3 лантаном или мишметаллом в вакууме при 1600 °C. Используют также карботермич. метод восстановления Sm2O3.
Наиб. значение для техники имеет металлический С. Его используют в производстве постоянных магнитов в виде сплавов с Со состава SmCo5 и SmCo17 (см. магнитные материалы). С. применяют для активации оксидных катодов, в производстве люминофоров, синтетич. железных гранатов, спец. стекол, керамич. конденсаторов, катализаторов, пигментов и др.
С. впервые выделил П. Лекок де Буабодран в 1879.
Лит. см. при ст. редкоземельные элементы.
Л. И. Мартыненко, С. Д. Моисеев, Ю. М. Киселев
Значения в других словарях
- Самарий — (лат. Samarium) Sm, химический элемент, атомный номер 62, атомная масса 150,4; редкоземельный металл; относится к лантаноидам (См. Лантаноиды). Большая советская энциклопедия
- самарий — орф. самарий, -я (хим.) Орфографический словарь Лопатина
- Самарий — Sm, химический элемент III группы периодической системы, атомный номер 62, атомная масса 150,36; относится к редкоземельным элементам; металл. Выделен французским химиком П. Лекоком де Буабодра-ном в 1879 г. Судьба эпонимов. Словарь-справочник
- САМАРИЙ — САМАРИЙ (символ Sm), серо-белый химический элемент, металл, относится к ЛАНТАНОИДАМ. Был впервые обнаружен спектроскопическим методом в 1879 г. Его основные руды — МОНАЦИТ и бастнезит. Научно-технический словарь
- Самарий — (Samarium), Sm (a. samarium; н. Samarium; ф. samarium; и. samario), — хим. элемент III группы периодич. системы Mенделеева, относится к лантаноидам, ат. н. 62, ат. м. 150,36. Природный C. Горная энциклопедия
- самарий — САМАРИЙ -я; м. Химический элемент (Sm), металл, относящийся к лантаноидам (в виде сплавов применяется в электротехнике). Толковый словарь Кузнецова
- Самарий — (Sm) — один из наиболее редких и потому столь мало исследованных химических элементов, что в настоящее время можно даже сомневаться в его химической самостоятельности. Энциклопедический словарь Брокгауза и Ефрона
- САМАРИЙ — САМАРИЙ (лат. Samarium) — Sm, химический элемент III группы периодической системы, атомный номер 62, атомная масса 150,36; относится к лантаноидам. Металл, плотность 7,536 г/см3, tпл 1072 °C. Большой энциклопедический словарь
- самарий — самарий м. Редкоземельный химический элемент, металл, соединения которого применяются в светотехнике. Толковый словарь Ефремовой
