Скраупа реакция
СКРАУПА РЕАКЦИЯ (Скраупа синтез)
получение хинолинов взаимод. первичных ароматич. аминов с глицерином в присутствии дегидратирующего агента и окислителя:
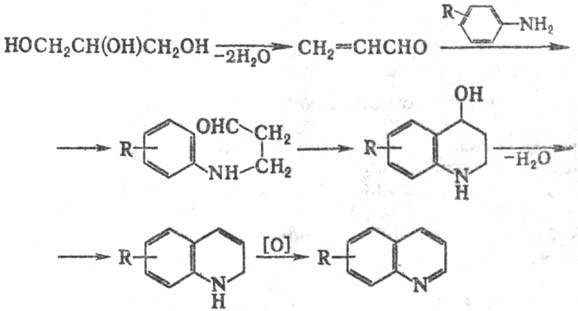
В качестве дегидратирующего агента используют H2SO4 (концентрация 60–70%), в качестве окислителя-обычно ArNO2 с Ar как у исходного амина.(применяют также I2, FeCl3, SnCl4, м-O2NC6H4SO3H и др.). Добавление в реакц. смесь FeSO4, CH3COOH, а также замена ароматич. амина на соответствующий ацетамид обеспечивают регулируемость процесса, который в некоторых случаях протекает бурно.
Замена глицерина непосредственно на акролеин обычно приводит к значит. осмолению продуктов. Однако замещенные производные акролеина и их ацетали, винилкетоны, и соед., образующие их в условиях реакции, реагируют по схеме С. р., напр.:
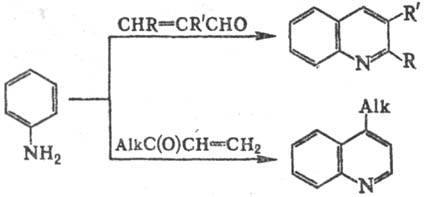
В реакцию вступают мн. замещенные ароматич. амины [лишь такие заместители, как CH3C(O), CH3O, CN, F в некоторых случаях в условиях С. р. отщепляются]. Mo-но-орто-замещенные анилины обычно образуют 8-замещен-ные хинолины, пара-замещенные — хинолины с заместителем в положении 6. мета-Замещенные анилины образуют 5- и(или) 7-замещенные хинолины. При этом дезактивирующие и мета-ориентирующие заместители (напр., NO2) благоприятствуют замыканию цикла по положению 2 с образованием 5-замещенных хинолинов; сильные активирующие и орто(пара)-ориентирующие группы (напр., OCH3) способствуют замыканию цикла по положению 6 с образованием 7-замещенных хинолинов. В остальных случаях образуются смеси изомеров. Соотношение изомерных хинолинов иногда зависит от концентрации кислоты. Так, в присутствии 60%-ной H2SO4 м-хлоранилин образует смесь 5- и 7-хлорхинолинов в соотношении 1:1,4, а с 80%-ной — в соотношении 1:3,9.
Ди-орто-замещенные анилины не вступают в С. р. Из 3,4-дизамещенных анилинов образуются два изомерных хинолина, причем наличие ориентантов 1-го рода благоприятствует образованию 6,7-производных. Ароматич. диамины реагируют с двумя эквивалентами глицерина с образованием фенантролинов.
Аминопроизводные нафталина, антрацена, фенантрена и др. конденсированных ароматич. соед. в условиях С. р. образуют т. наз. арохинолины [напр., 1-нафтиламин образует бензо[h]хинолин (формула I), 2-нафтиламин-бензо[f]хи-нолнн (II)]:
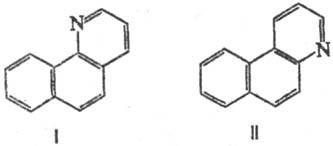
Стремление к замыканию кольца по положению 1 настолько сильно, что галоген или группа NO2 в положении 1 в 2-нафтиламинах отщепляются в ходе реакции (в результате образуются арохинолины формулы I).
В условиях С. р. аминопроизводные ряда тиофена, фурана и пиридина частично разлагаются и обычно дают низкие выходы соответствующих; конденсир. гетероциклич. систем, напр.:
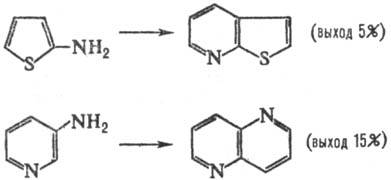
Обычно С. р. осуществляют, нагревая смесь реагентов в течение неск. часов (реже — минут). Затем смесь охлаждают, приливают воду (иногда водный раствор NaOH), выделяют конечный продукт перегонкой с водяным паром. Выходы 40–90%. Осн. побочные продукты — смолы, продукты гидролиза замещенных ароматич. аминов, изомерные конденсир. системы.
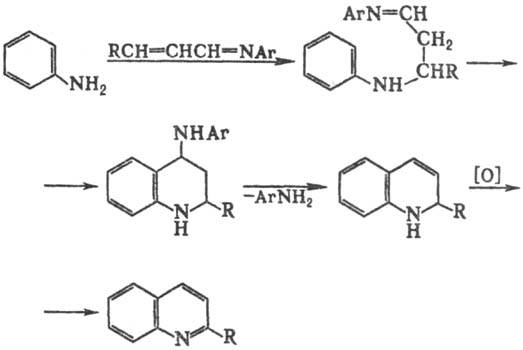
Одна из модификаций С. р. — использование основания Шиффа; в этом случае замыкание цикла сопровождается элиминированием амина вместо H2O:
Синтез хинолинов из ароматич. аминов и глицерина в среде 85%-ной H3PO4 наз. модификацией Йейла.
С. р. широко используют в препаративной практике, для получения фармацевтич. препаратов, фотосенсибилизаторов и др. Реакция открыта 3. Скраупом в 1880.
Лит.: Манске Р., Кулка М., в сб.: Органические реакции, пер. с англ., сб. 7, М., 1956, с. 100–145; Общая органическая химия, пер. с англ., т. 8, М., 1985, с. 198–201.
Г. И. Дрозд
Значения в других словарях
- Скраупа реакция — Синтез хинолина (III), его аналогов и производных взаимодействием анилина (1), соответственно его аналогов и производных... Большая советская энциклопедия
