свинца нитрат
СВИНЦА НИТРАТ Pb(NO3)2
бесцветные кристаллы кубич. сингонии (а = 0,784 нм, z = 4, пространственная группа Ра3); плотн. 4,538 г/см3; 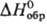 −451,75 кДж/моль;
−451,75 кДж/моль;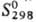 217,9 Дж/(моль∙К). При нагр. выше 200 °C начинает разлагаться без плавления с выделением NO2 и O2 и последоват. образованием оксонитратов Pb(NO3)2 ∙ 2PbO, Pb(NO3)2 ∙ 5PbO и оксида PbO при 500–550 °C. Растворимость в воде (г в 100 г):45,5 (10 °C), 58,5 (25 °C), 91,6 (60 °C) и 116,4 (80 °C). Хорошо раств. в гидразине, аммиаке, пиридине и форма-миде, не раств. в этаноле, ацетоне и неполярных растворителях. В водных растворах диссоциирован, при избытке ионов NO3−образует нитратокомплексы [Pb(NO3)3]−, [Pb(NO3)4]2− и [Pb(NO3)6]4−. Степень гидролиза С.н. в растворе составляет 0,05–0,15. При повышении pH раствора образуются гидроксо-нитраты переменного состава Pb(OH)x(NO3)y, некоторые из них выделены и в твердом состоянии. Получен ряд безводных и гидратированных оксонитратов xPb(NO3)2∙yPbO • zH2O.
217,9 Дж/(моль∙К). При нагр. выше 200 °C начинает разлагаться без плавления с выделением NO2 и O2 и последоват. образованием оксонитратов Pb(NO3)2 ∙ 2PbO, Pb(NO3)2 ∙ 5PbO и оксида PbO при 500–550 °C. Растворимость в воде (г в 100 г):45,5 (10 °C), 58,5 (25 °C), 91,6 (60 °C) и 116,4 (80 °C). Хорошо раств. в гидразине, аммиаке, пиридине и форма-миде, не раств. в этаноле, ацетоне и неполярных растворителях. В водных растворах диссоциирован, при избытке ионов NO3−образует нитратокомплексы [Pb(NO3)3]−, [Pb(NO3)4]2− и [Pb(NO3)6]4−. Степень гидролиза С.н. в растворе составляет 0,05–0,15. При повышении pH раствора образуются гидроксо-нитраты переменного состава Pb(OH)x(NO3)y, некоторые из них выделены и в твердом состоянии. Получен ряд безводных и гидратированных оксонитратов xPb(NO3)2∙yPbO • zH2O.
В лаборатории С.н. получают растворением Pb, PbO или PbCO3 в HNO3 или электролизом свинцовых анодов в растворе NaNO3, в промышленности-растворением гранул Pb в слабой HNO3. С.н. ограниченно применяют для получения др. соед. свинца; компонент пиротехн. составов.
Известны алкил- и арилпроизводные нитрата Pb(IV) состава (C2H5)3PbNO3, (C6H3)2Pb(NO3)2 и т. п. С.н. токсичен; ПДК 0,01 МГ/М3
П. М. Чукуров
