тетрацианохинодиметан
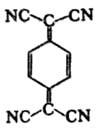
ТЕТРАЦИАНОХИНОДИМЕТАН (7,7,8,8-тетрацианохинодиметан, ТЦХМ, TCNQ)
мол. м. 204; желто-зеленые кристаллы. Молекула плоская; параметры кристаллич. решетки: а = 0,891 нм, b = 0,706 нм, с = = 1,6395 им, β = 98,54°, z = 2. Плоти. 1,315 г/см3, т. пл. 296–298 °C (из ацетонитри-ла), т. возг. >250 °C (в вакууме-200 °C). Хорошо раств. в бензоле, CHCl3, ацето-нитриле, ТГФ, этилацетате, трудно — в спиртах, не раств. в воде. В твердом виде на воздухе устойчив, в растворах чувствителен к влаге.
Окислит.-восстановит. свойства Т.: потенциал первой полуволны восстановления E1/2= + 0,127 В, потенциал второй полуволны восстановления Е1/2 = — 0,29 В.
Т. легко вступает в реакции 1,6-присоединения и замещения по группам CN, напр.:
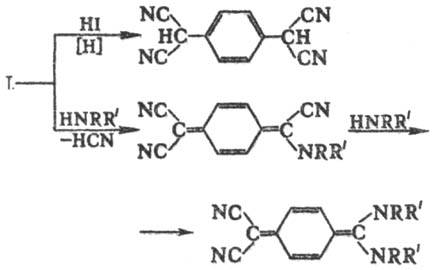
Как сильная кислота Т. склонен к комплексообразованию с разл. основаниями Льюиса. С некоторыми соед. — донорами электронов (D, напр. дибензотетратиафульваленом, антраценом) Т. образует мол. комплексы с переносом заряда типа D ∙ TCNQ0 (см. молекулярные комплексы), кристаллы которых содержат бесконечные стопки чередующихся молекул D и TCNQ. С разл. металлич., орг. и металлоорг. катионами D+ Т. образует простые или сложные ион-радикальные соли, соотв. 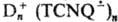 иотносящие
иотносящие 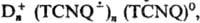
В первых электрон полностью перенесен с молекулы донора на молекулу TCNQ и электронный спектр их растворов содержит полосы поглощения катионов D+ и анион-радикала 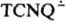 ; сложные ион-радикальные соли в растворе диссоциируют с образованием катиона донора, анион-радикала
; сложные ион-радикальные соли в растворе диссоциируют с образованием катиона донора, анион-радикала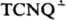 и нейтральной молекулы TCNQ0. Осн. методы получения анион-радикальных солей — прямое взаимод. металлов с Т., обменные реакции солей доноров и солей Т., восстановление Т. в присутствии катионов, напр.:
и нейтральной молекулы TCNQ0. Осн. методы получения анион-радикальных солей — прямое взаимод. металлов с Т., обменные реакции солей доноров и солей Т., восстановление Т. в присутствии катионов, напр.:
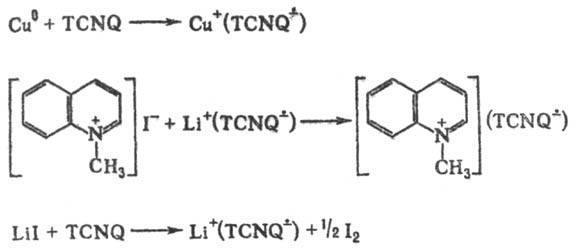
Получают Т. конденсацией малонодонитрила с цикло-гексан-1,4-дионом с послед. бромированием и дегидробромированием в присутствии пиридина.
Т. и его соли-активные материалы в источниках тока и разл. устройствах с регистрацией оптич., электрич. и магн. величин (датчики давления, электрохромные индикаторы).
Лит.: Шибаева Р. П., Атовмян П. О., "Ж. структурн. химии", 1972, т. 1, № 3, с. 546; Бесиалов Б. П., Титов В. В., "Успехи химии", 1975, т, 44, в. 12. с. 2249–83; Acker D. S., Hertler W. R., "J. Amer. Chem. Soс.", 1962, v. 84, № 17, p. 3370–74; Shchegolev I. F., "Physics stat solid"(a), 1972, v. 12, p. 9; Torrance J. R., "Ace. Chem. Res.", 1979, v. 12, № 3, p. 79–85.
Р. Н. Любовская
