тетрацианоэтилен
ТЕТРАЦИАНОЭТИЛЕН (NC)2C=C(CN)2
мол. м. 128,09; бесцветные кристаллы моноклинной сингонии (а = 0,751 нм, b = 0,621 нм, с = 0,700 нм, β = 97,17°, z = 2, пространственная группа P21/n); т. пл. 201–202 °C (в запаянном капилляре), т. кип. 223 °C, при температуре выше 120 °C возгоняется; плота. 1,318 г/см3; 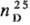 1,560; уравнение температурной зависимости давления пара: lgp (мм рт. ст.) = 11,67 — 4250/Т;
1,560; уравнение температурной зависимости давления пара: lgp (мм рт. ст.) = 11,67 — 4250/Т; 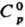 0,849 кДж/(кг∙К); ΔHвозг 81,2 кДж/моль, ΔH0сгор −2,98 кДж/моль,
0,849 кДж/(кг∙К); ΔHвозг 81,2 кДж/моль, ΔH0сгор −2,98 кДж/моль, 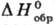 −623,8 кДж/моль; ε 2,93–3,60.
−623,8 кДж/моль; ε 2,93–3,60.
Практически не раств. в воде, раств. во многих органических растворителях. Термически стабилен до 600 °C; при 800 °C распадается на дициан (CN)2 и дицианоацетилен NCC==CCN. С донорами электронов (циклогексен, пиридин, а также бензол, нафталин, флуорен, пирен и др. арены) образует интенсивно окрашенные комплексы с переносом заряда, в которых выступает в роли кислоты Льюиса.
Т. вступает в реакции циклоприсоединения (реакцию с 1,3-диенами часто используют для характеристики последних, в т. ч. нестабильных и трудно выделяемых), напр.:
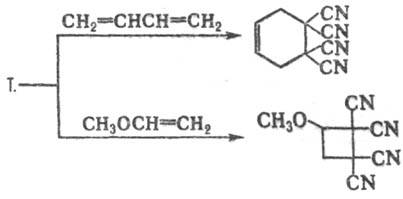
Т. восстанавливается до 1,1,2,2-тетрацианоэтана, из которого далее м. б. получены гетероциклич. соед.; легко вступает в реакции с разл. нуклеофилами, напр.:
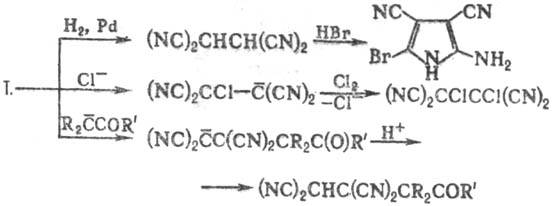
Для Т. характерны реакции замещения одной или двух цианогрупп на OH, OR, амино, арил и др., напр.:
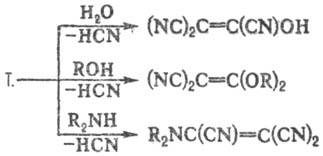
Продукт гидролиза Т. трицианоэтенол-сильная кислота, выделена лишь в виде солей.
При взаимодействии Т. с H2O2 образуется кристаллич. оксиран. В присут. металлов, металлокомплексов, спиртов, фенолов, аминов или ароматич. соед. при 160–180 °C Т. полимеризуется (в отличие от акрилонитрила полимеризация протекает по группе C=N); полимеры обладают свойствами полупроводников и каталитич. свойствами.
Получают Т. из малонодинитрила: 2CH2 (CN)2 + 2S2Cl2 → Т. + 4HCl + 4S; из дихлорфумародинитрила: NCC(Cl)=C(Cl)CN + 2HCN → T. Для получения Т. в больших масштабах м. б. использован синтез из тетрациано-1,4-дитиина:
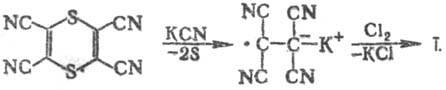
В лаборатории Т. получают из малонодинитрила по реакции:
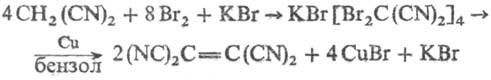
Используют Т. в качестве полупродукта в орг. синтезе И при получении лек. веществ. По токсичности Т. близок к KCN.
Лит.: Физер Л., Физер М., Реагенты для органического синтеза, пер. с англ., т. 3, М., 1970, с. 314–18; Gmelins Handbuch der anorganischen Chemie, 8 Aufl., Bd 14, Tl Dl, В., 1974, S. 107–15; Kirk-Othmer encyclopedia, 3 ed., v. 6, N. Y., 1978, p. 625–33.
С. К. Смирнов
