тетрахлорэтаны
ТЕТРАХЛОРЭТАНЫ
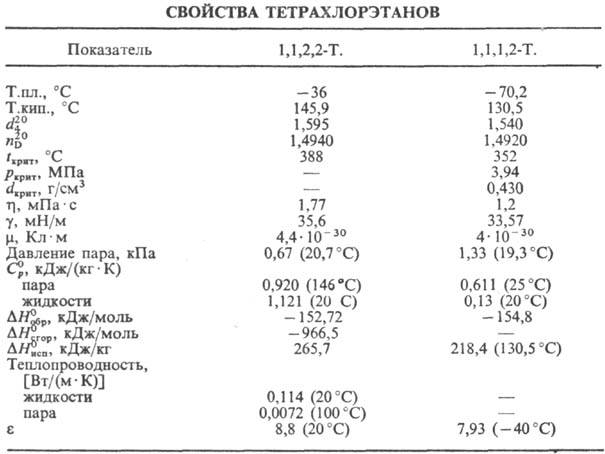
мол. м. 167,85. Различают 1,1,2,2-Т. CHCl2CHCl2 и 1,1,1,2-Т. CCl3CH2Cl; бесцв. жидкости (см. табл.) со сладковатым запахом; хорошо раств. во мн. органических растворителях. Для 1,1,2,2-Т. растворимость в воде (% по массе): 0,13 (20 °C), 0,34 (55,6 °C), растворимость воды в 1,1,2,2-Т. 0,11 (25 °C); образует азеотропную смесь с водой (т. кип. 93,7 °C, 29,3% H2O по массе); энергии связей (кДж/моль) С—H 409,2, С —Cl 310,9, С —С 352,7. Для 1,1,1,2-Т. растворимость в воде (% по массе): 0,109 (20 °C), 0,125 (50 °C), растворимость воды в 1,1,1,2-Т. 0,056 (25 °C); энергии связей (кДж/ моль): С—H (для группы CH2Cl) 409,29, С —Cl (для CCl3 и CH2Cl) соотв. 293,7 и 335,1, С —С 336,8.
Т. реагируют с хлором в жидкой фазе в присутствии инициаторов (порофоров) при 80–90 °C с образованием пентахлор-этана и далее гексахлорэтана. При дегидрохлорировании щелочными агентами при 90–100 °C либо в паровой фазе при 400–500 °C или на катализаторе (Al2O3, BaCl2 на носителе и др.) при 300–350 °C образуется трихлорэтилен. 1,1,2,2-Т. дехлорируется в присутствии H2 над Ni при 300–350 °C или над Zn с водяными парами.
В промышленности 1,1,2,2-Т. получают хлорированием ацетилена в жидкой фазе при 100–120 °C в реакторах барботажного типа, заполненных железными (чугунными) шарами; количество хлора поддерживается на уровне 5–15% избытка по отношению к ацетилену. После нейтрализации, промывки и осушки продукт содержит 97–98% 1,1,2,2-Т. Применяют его для производства трихлорэтилена. 1,1,2,2-Т. — трудногорючий продукт, т. самовоспл. 474 °C; ПДК 6 мг/м ,. в водоемах 0,2 мг/л.
1,1,1,2-Т. м. б. получен хлорированием винилиденхлорида в жидкой фазе в присутствии 0,01–0,1% РеCl3 при 20–30 °C.
Лит.: Промышленные хлорорганические продукты. Справочник, под ред. Л. А. Ошина, М., 1978; Трегер Ю. А., Карташов Л. М., Кришталь H. Ф., Основные хлорорганические растворители, М., 1984.
Ю. А. Трегер
