Ван-дер-Ваальса уравнение
ВАН-ДЕР-ВААЛЬСА УРАВНЕНИЕ
уравнение состояния реального газа. Для n молей газа, имеющего объем V при температуре Т и давлении р. имеет вид:
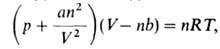
где R — газовая постоянная, а и b-постоянные Ван-дер-Ваальса, характерные для данного вещества. Член an2/V2 учитывает притяжение молекул газа (уменьшение давления) вследствие межмолекулярных взаимод., член nb-отталкивание молекул на близких расстояниях из-за наличия у них "собственного объема". Для разреженных газов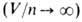 В. у. принимает вид: pV = nRT (см. Клапейрона — Менделеева уравнение). Постоянные а и b определяют экспериментально, напр. по параметрам критич. точки.
В. у. принимает вид: pV = nRT (см. Клапейрона — Менделеева уравнение). Постоянные а и b определяют экспериментально, напр. по параметрам критич. точки.
В. у. — простейшее уравнение состояния, позволяющее определять точку фазового перехода газ — жидкость и критич. температуру, выше которой вещество может находиться только в газообразном состоянии. Однако В. у. является приближенным и количественно описывает некоторые свойства газа лишь при высоких Т и низких р. Оно даже качественно не описывает многие свойства реального газа, напр. зависимость изохорной теплоемкости от плотности. Термодинамич. свойства газов м. б. рассчитаны с достаточной точностью на основе вириаль-ного уравнения состояния.
Уравнение было предложено И. Д. Ван-дер-Ваальсом в 1873.
Лит. см. при ст. газы.
М. А. Анисимов
Значения в других словарях
- ВАН-ДЕР-ВААЛЬСА УРАВНЕНИЕ — Одно из первых уравнений состояния реального газа. Предложено в 1873 голл. физиком Я. Д. Ван-дер-Ваальсом (J. D. van der Waals). Для моля газа, имеющего объём V при темп-ре Т и давлении р, имеет вид: (p+a/V2)(V-b)=RT... Физический энциклопедический словарь
- Ван-дер-Ваальса уравнение — Одно из первых уравнений состояния реального газа, предложенное голландским физиком Я. Д. Ван-дер-Ваальсом (1873): Здесь: р — давление газа; Т — его температура; V̅ — объём одного моля вещества; R — универсальная Газовая постоянная; а и b — константы... Большая советская энциклопедия
- ВАН-ДЕР-ВААЛЬСА УРАВНЕНИЕ — ВАН-ДЕР-ВААЛЬСА УРАВНЕНИЕ — предложенное Й. Д. Ван-дер-Ваальсом (1873) — уравнение состояния реального газа, учитывающее конечность объема молекул и наличие межмолекулярных сил притяжения; для одного моля имеет вид: (p+a/V2)(V-b) V = RT,где... Большой энциклопедический словарь
