триорганоарсины
ТРИОРГАНОАРСИНЫ (третичные арсины)
соед. общей формулы R3As. Триалкиларсины, как правило, жидкости, три-ариларсины обычно твердые вещества (см. табл.); раств. в органических растворителях, не раств. в воде [за исключением (CH3)3As].
Т. обладают высокой термостабильностью [напр., (CH3)3As и (CF3)3As разлагаются при температуре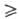 350 °C], относительно легко присоединяют O2, S, Se, Hal2, образуя соответствующие производные As(IV) и As(V). Т. — слабые основания, их соли с HHal и комплексы с кислотами Льюиса неустойчивы. Известны относительно устойчивые комплексы Т. с галогенидами и карбонилами переходных металлов, напр. [(C6H5)3As]2-Ru(CO)3, C6H4[As(CH3)2]2-Fe(CO)3. При действии RHal Т. образуют соед. арсония типа [R4As]+Hal−. Связь As—С расщепляется при действии нуклеофилов на перфторалкил- и хлорвиниларсины, щелочных металлов, O2 и H2 при высоких температурах, а также при электролизе или радиолизе. Взаимодействие Т. с азидами приводит к иминоарсинам, напр.: (C6H5)3As + N3CN:(C6H5)3As = NCN + N2.
350 °C], относительно легко присоединяют O2, S, Se, Hal2, образуя соответствующие производные As(IV) и As(V). Т. — слабые основания, их соли с HHal и комплексы с кислотами Льюиса неустойчивы. Известны относительно устойчивые комплексы Т. с галогенидами и карбонилами переходных металлов, напр. [(C6H5)3As]2-Ru(CO)3, C6H4[As(CH3)2]2-Fe(CO)3. При действии RHal Т. образуют соед. арсония типа [R4As]+Hal−. Связь As—С расщепляется при действии нуклеофилов на перфторалкил- и хлорвиниларсины, щелочных металлов, O2 и H2 при высоких температурах, а также при электролизе или радиолизе. Взаимодействие Т. с азидами приводит к иминоарсинам, напр.: (C6H5)3As + N3CN:(C6H5)3As = NCN + N2.

Т. получают действием RMgHal на As2O3 или AsX3 (X = Hal, OR), реакцией R2Zn с AsCl3, совместным действием Na и RHal на AsHal3, присоединением арсинов RnAsX3-n (X = H, Hal; n = 0–2) к непредельным соединениям, трис-(Полифторалкил)арсины получают алкилированием As полифториодалканами.
Триалкиларсины используют в электронной промышленности для легирования эпитаксиальных слоев.
Лит. см. при ст. мышьякорганические соединения.
Г. И. Дрозд
